甘氨酸铁螯合物结构式的验证分析
2014-02-27
(上海德邦牧业有限公司,上海201108)
1 定性分析
1.1 红外光谱分析
通过红外光谱能反映分子内化学键的振动和转动,也称为分子振动转动光谱,从而定性判断甘氨酸与铁离子是否发生了螯合反应。化学键不同,其红外吸收峰的位置和形状不同,从而可对物质进行定性分析;根据红外吸收峰的强度可对物质进行定量分析;此外,红外光谱还能提供有关分子结构的信息。因此,红外光谱具有定性、定量和定结构的作用,是分析化学的重要技术手段。红外光谱在微量金属有机螯合物领域也得到了广泛应用。
由于红外吸收的复杂性,直接给出甘氨酸金属螯合物形成的证据并不容易。一般是通过将纯甘氨酸与甘氨酸金属螯合物的红外光谱作比较,间接证明甘氨酸金属螯合物的形成。甘氨酸中主要的官能团为羧基和氨基,主要是通过这两个官能团特征红外吸收峰的变化来研究螯合物的形成。
甘氨酸与某甘氨酸亚铁红外光谱吸收峰比较见图1、表1。
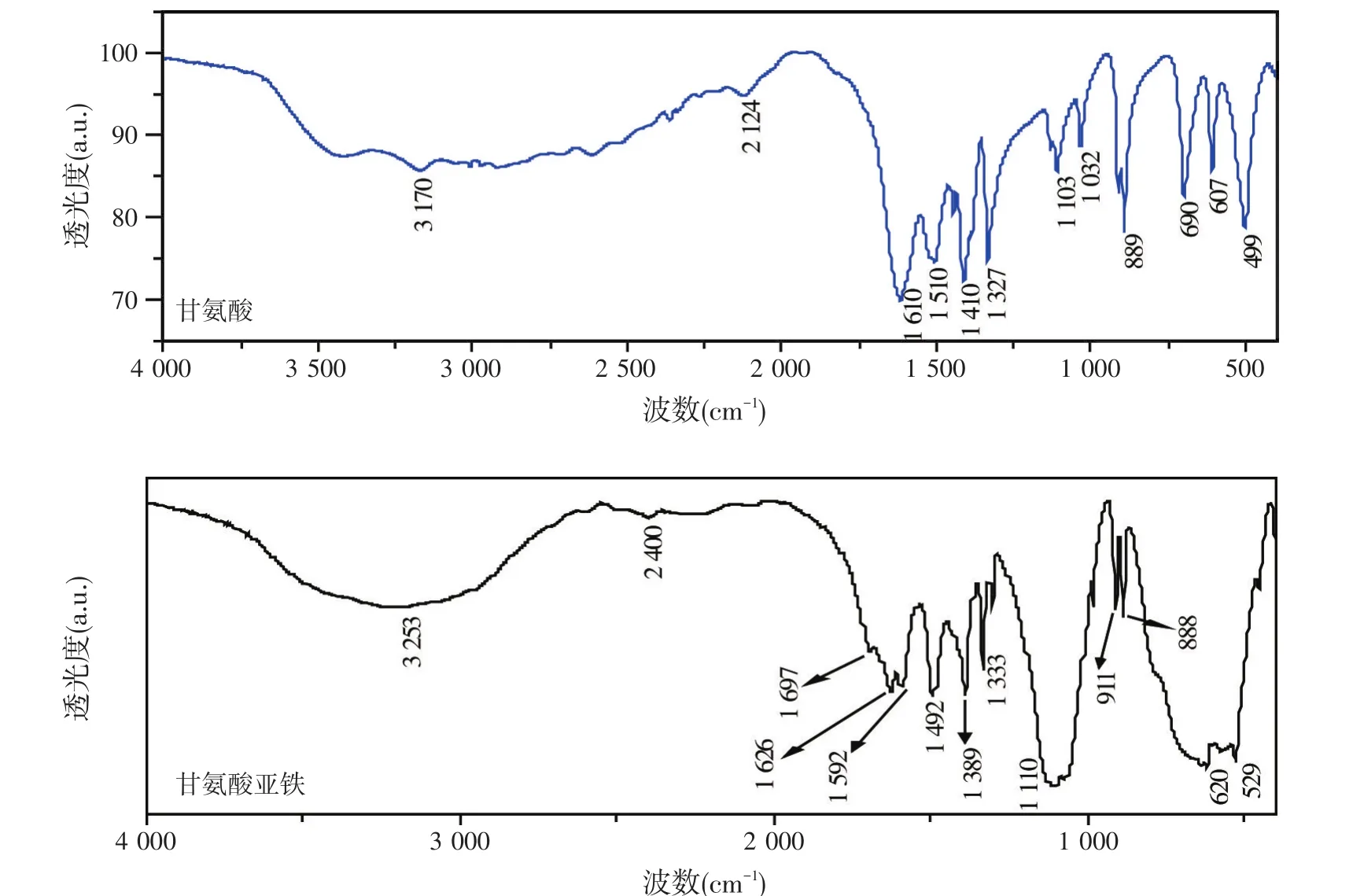
图1 红外光谱
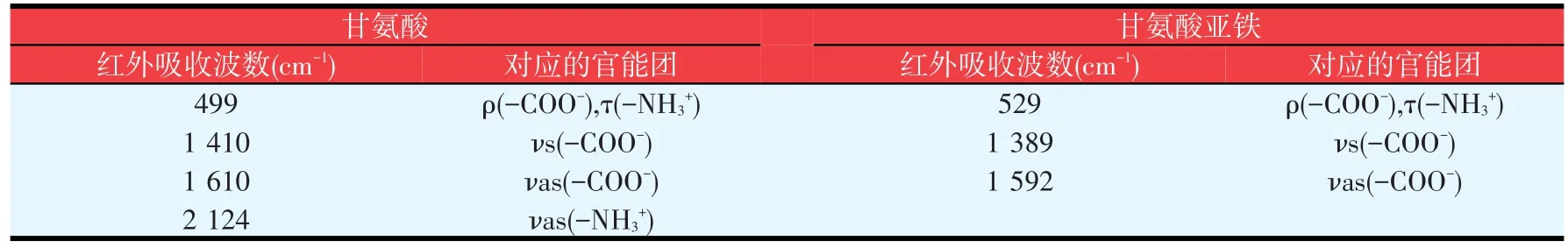
表1 红外光谱吸收峰分析
甘氨酸在499 cm-1处有一个强的红外吸收峰,这对应甘氨酸中-COO-和-NH3+的特征红外吸收峰。而甘氨酸亚铁的红外光谱图中499 cm和2 124 cm处-COO-和-NH3+的吸收峰发生较大漂移,这说明产品中的甘氨酸已与Fe2+形成了配位键。甘氨酸在1 410 cm和1 610 cm处的吸收峰分别为羧基(-COO-)的对称与不对称伸缩振动的吸收。2 124 cm为-NH3+的不对称伸缩振动的红外吸收峰。而甘氨酸亚铁上的羧基在1 610 cm处的不对称伸缩吸收峰发生红移,出现在1 592 cm。
所以通过红外光谱分析,观测-NH3+和-COO-的位移变化来推断甘氨酸和铁元素是否发生了螯合反应。从而视为甘氨酸铁螯合物有效的定性方法。
1.2 拉曼光谱分析
拉曼光谱为分子光谱,是分子对光的散射。当激发光照射到分子表面时,与分子相互作用,大部分的光子只改变方向发生反射,少部分光子不仅改变光的传播方向,且频率也于激发光不同,这种散射称为拉曼散射。拉曼散射光与入射光频率的差值(±Δυ)称为拉曼位移,它与分子振动转动能级相关,分子中不同的化学键有不同的振动能级,相应的拉曼位移也是特征的,因此,拉曼光谱可以用于分子结构定性、定量分析,它与上述的红外光谱互补,可得到较完整的分子振动能级跃迁信息。本试验以甘氨酸为对照,测定甘氨酸在900 cm-1处有一个明显的吸收峰(见图2)。而甘氨酸铁螯合物的吸收峰产生了相应的位移,这是由于甘氨酸中的-COO-和-NH3+与铁离子发生了螯合反应。拉曼光谱作为红外光谱的一种有效补充,从而进一步证明甘氨酸与铁离子发生了螯合反应。

图2 拉曼光谱
1.3 XRD衍射分析
XRD也称之为X射线衍射,通过对物质进行X射线衍射,分析其衍射图谱,从而定性分析物质的内部结构。目前X射线衍射已经成为研究晶体物质和某些非晶态物质微观结构的有效方法。本试验通过XRD分析甘氨酸亚铁的晶体特性。通过图3可知,甘氨酸铁的XRD衍射图谱峰值比较直,结晶程度高,晶型好。
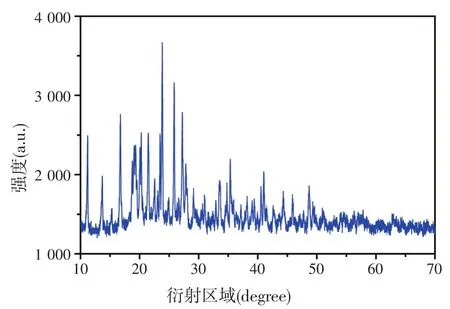
图3 甘氨酸铁XRD衍射图谱
通过上述XRD衍射图谱可知,甘氨酸铁为晶体结构。结合上述红外光谱、拉曼光谱,得出甘氨酸和硫酸亚铁不是简单的混合,而是发生相应的化学反应,其中Fe2+与甘氨酸配体之间的化学键主要为配位键。并且呈现较好的晶体结构。
2 定量分析
认识一个新的物质,主要通过定性和定量两个层面来分析,甘氨酸亚铁作为一种化工合成产品,定性层面上已经做了系统的分析论证,结合定性的结果,表2为试验检测其内部相应元素的含量,以综合进行分析论证。

表2 元素测定结果
3 结论
通过上述检测推断出甘氨酸铁的结构式为:
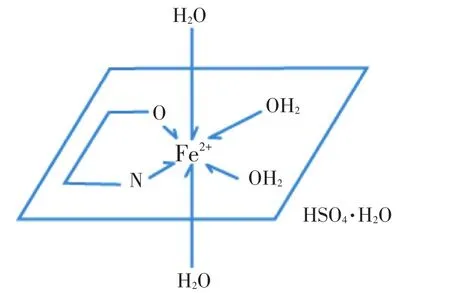
Fe2+核外有6个空轨道,其中两个空轨道分别与甘氨酸中的O和N进行结合,其他四个位置分别与四个结晶水进行结合。由于甘氨酸和铁在1:1 mol螯合情况下形成的为络阳离子,核外必然带有一个阴离子硫酸根离子,再带一个结晶水。所以甘氨酸铁的分子式为:NH3CH2COOHFe·SO4·SO4·H2O。由表3可知甘氨酸铁理论含量。

表3 甘氨酸铁理论含量
