沸石处理高氨氮景观水吸附特性实验研究
2013-11-09王小强马晓颖
王小强 马晓颖
(1.中煤西安设计工程有限责任公司,陕西西安 710054;2.中国电力顾问集团西北电力设计院,陕西西安 710075)
1 概述
随着社会快速发展和人们生活居住条件日益改善,景观水(公园、居住小区、公共场所的水景及城市内的河流湖泊)慢慢地融入了人们的生活。但是,大部分景观水体,系统封闭,缺乏循环系统,因此水体常处于静止状态,再加上景观水体水位浅,使得整个水生态系统更加脆弱,自净能力严重不足。因此景观水体中氨氮、磷含量通常较高,给藻类生长提供了大量营养物质,致使水中藻类爆发,富营养化趋势不断加重。若长时间未采取有效措施,不但使得景观水体观赏效果大大下降,更有甚者会对周围居民正常生活造成严重影响,甚至威胁人体健康。因此,合理有效的改善景观水体水质,快速经济地恢复其在城市生活中的生态功能和美学价值,成为城市生态环境建设及可持续发展的一个亟待解决的重要问题[1-10]。而其中如何去除景观水体中的高氨氮又成为景观水处理中的研究热点。
处理景观水体常用到的方法有物理覆盖、化学修复、生物修复等,其中物理覆盖常用的覆盖材料有砾石、沙子及一些矿石填料如沸石、陶粒、方解石等。很多研究学者研究结果表明,沸石通过吸附、拦截等作用对氨氮去除效果明显,去除率明显高于其他材料;另一方面,我国沸石储量相对较大,开采工艺简单,价格便宜,吸附饱和失效后可通过简单方法再生以便重复使用,且易于实现原位处理。因此,同其他处理方法及覆盖材料相比,具有成本低,经济高效,便于实现等众多优点[11]。天然沸石以二氧化硅为其主要化学成分。天然沸石是一种含水铝硅酸盐矿物,其空间网架状结构及蕴含丰富空腔和孔道的特性决定了可以吸附并贮存大量分子[12,13]。本研究以景观水体为实验对象,考察了沸石去除景观水体中高氨氮的吸附特性,以期为工程应用提供理论依据与技术支持。
2 实验材料与方法
2.1 实验材料
本实验研究选用的天然斜发沸石滤料买自河南巩义夹津口海宇填料生产厂。实验开始前,用蒸馏水将所购沸石洗净,并在105℃的烘箱内干燥5 h,然后置于干燥器中备用。
原水:取自西安某景观水,其主要化学成分如表1所示。
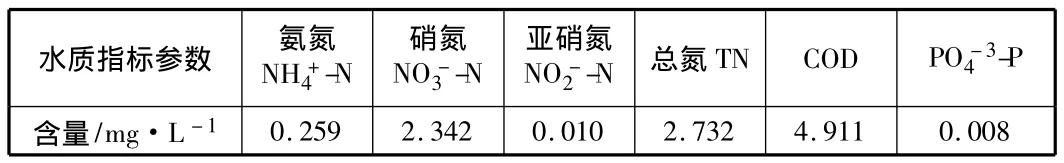
表1 某景观水原水水质
2.2 实验方法
1)沸石去除氨氮随时间变化:动力学实验研究。以50 mL的离心管为反应容器,将1 g准备好的沸石填料置于其中,加入浓度为50 mg/L氨氮(氯化铵)溶液20 mL,置于恒温摇床震荡(温度设定室温 25 ℃),实验开始后分别于 5 min,10 min,30 min,1 h,2 h,6 h等时刻取水样,直至达到去除平衡,经0.45 μm滤膜过滤后测定水样中剩余氨氮浓度值,直到沸石吸附氨氮达到平衡为止。
2)初始氨氮浓度对沸石吸附的影响:等温吸附实验研究。同样以50 mL的离心管为反应容器,将1 g准备好的沸石填料置于其中,在不同反应容器中加入初始浓度不同的氨氮(氯化铵)溶液20 mL,初始浓度分别为 10 mg/L,25 mg/L,50 mg/L,80 mg/L,100 mg/L,200 mg/L,250 mg/L,300 mg/L。置于恒温摇床震荡(温度设定为25℃),根据1)实验测定结果,反应振荡进行72 h后取出反应容器,将水样经0.45 μm滤膜过滤后测定水样中剩余氨氮浓度值。
3)不同温度对沸石吸附氨氮效果的影响。以50 mL的离心管为反应容器,将1 g准备好的沸石填料置于其中,加入浓度为50 mg/L氨氮(氯化铵)溶液20 mL,置于恒温摇床震荡,设置恒温震荡摇床温度分别为10℃,15℃和25℃,反应振荡进行72 h后取出反应容器,将水样经0.45 μm滤膜过滤后测定水样中剩余氨氮浓度值。
3 结果与讨论
3.1 沸石去除氨氮随时间变化:动力学研究
如实验方法1)中所述,每隔一定时间(5 min,10 min,30 min,1 h,2 h,6 h,12 h,24 h,36 h,72 h)取出置于25 ℃恒温震荡摇床上进行吸附动力实验研究的反应容器离心管,测定水样中剩余氨氮浓度值,计算其相应去除率,结果如图1所示。从图1中可以看出,初始阶段,沸石对氨氮吸附量迅速增加,振荡反应进行3 000 min后,随时间延长,吸附量增加速度减缓,此时最高去除率高于90%。
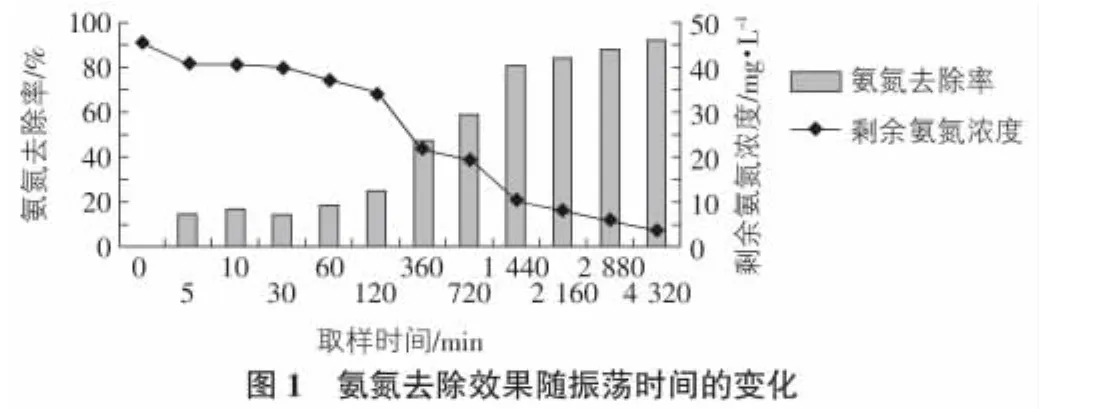
3.2 初始氨氮浓度对沸石吸附的影响:等温吸附研究
再如实验方法2)中所述,选取吸附时间为72 h,考察沸石投加量为1 g,25℃条件下,不同初始浓度的氨氮溶液(10 mg/L,25 mg/L,50 mg/L,80 mg/L,100 mg/L,200 mg/L,250 mg/L,300 mg/L)对吸附效果的影响,测定结果如图2所示。在图2中用q表示固体在溶液中吸附质吸附的能量大小,即吸附量,通过以下公式计算:
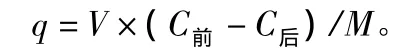
其中,q为沸石吸附量,mg/g;V为溶液体积,mL;C前为吸附前溶液浓度,mg/L;C后为吸附后溶液浓度,mg/L;M为沸石质量,g。
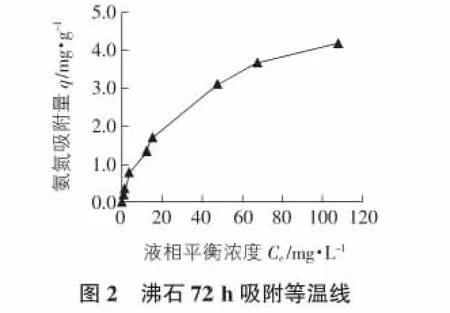
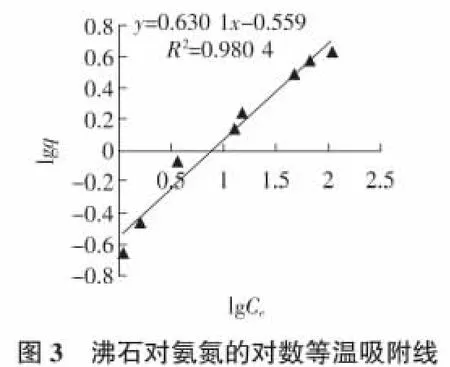
对照经典等温吸附公式弗罗因德利希(Freundlich)及朗格缪尔(Langmuir)公式与本实验研究结果对照(如图3,图4所示)。由图3,图4可见,研究结果更符合朗格缪尔(Langmuir)公式,因此,本研究所选取的沸石在设定实验条件下对NH+4的等温吸附公式可表示为q=Ce/(4.449 2+0.21Ce)。氨氮吸附极限值为4.642 3 mg/g。从动力学观点出发的朗格缪尔(Langmuir)等温吸附理论以单分子层吸附;吸附固体表面均匀;被吸附在固体表面上的分子相互之间无作用力;吸附平衡为动态平衡等为基本假设,认为固体表面对气体分子的吸附是单分子层吸附。但是该式中常数物理意义不明,只能算作经验公式,这是其用于溶液吸附时的最大缺点[7]。

3.3 不同温度对沸石吸附氨氮效果的影响
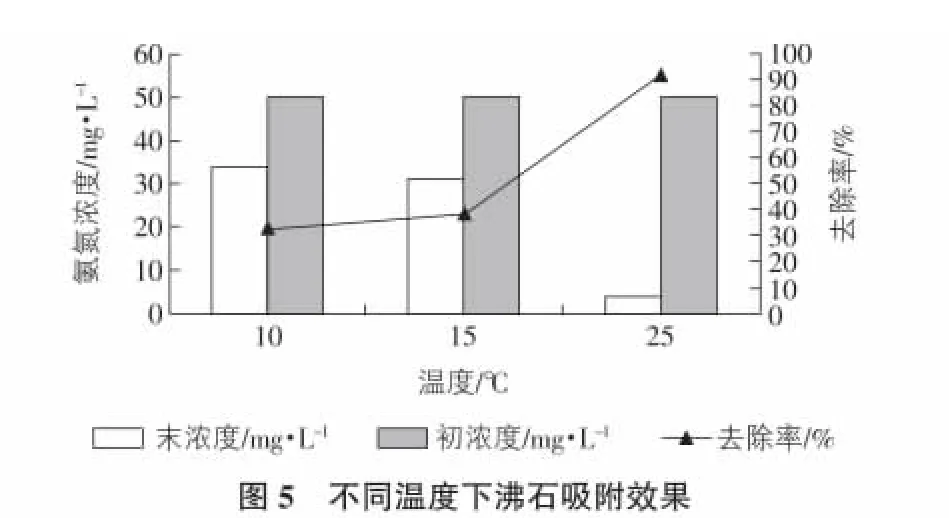
不同温度对沸石吸附氨氮效果的影响实验结果如图5所示。从图5中可以看出,在实验所选温度范围内(10℃,15℃和25℃),沸石的吸附量随反应温度升高而升高。从10℃变至15℃时,实验所选沸石对氨氮去除率随温度升高缓慢增加;温度为25℃时,去除率迅速达到93.4%。由此可见在实验所选三个温度中(10℃,15℃,25℃)25℃时,沸石对氨氮的去除率最高,最高去除率为93.4%。
4 结语
使用沸石对氨氮去除率可达90%以上;沸石对氨氮符合经典等温吸附模型Langmuir等温模型。本实验研究所选用的沸石对氨氮的吸附极限值为4.642 3 mg/g;实验所选取的三个温度中(10℃,15℃,25℃)25℃时,沸石对氨氮的去除率最高,最高去除率为93.4%。
[1]孙丽娟,费寿娥,曹绪峰.城市景观水生态修复方法研究进展与发展趋势[J].金陵科技学院学报,2008,24(2):77-80.
[2]梁燕珍,孙国萍,岑英华,等.生物技术在微污染景观水处理中的应用[J].环境科学与技术,2005,28(2):88-90.
[3]杜文华,芮 旻,陈 斌.城市景观水污染现状及处理技术[J].环境保护科学,2006(2):11-14.
[4]王 琳,李 季,康文力,等.城市景观水体的生物修复技术[J].安徽农业科学,2008,36(4):1569-1570,1572.
[5]孙 健.城市景观水体污染现状及其修复对策[J].鸡西大学学报,2009,9(5):149-150.
[6]李立欣,战 友.河湖底泥修复技术的研究进展[J].黑龙江环境通报,2008,32(4):27-29.
[7]张淑红,刘秀花,王 莉,等.景观水修复技术研究进展[J].商丘师范学院学报,2009,25(9):109-111,118.
[8]邹许鑫,罗卓英,吕 燕.浅论生态景观水体污染原因和治理方法[J].有色金属设计,2008,35(4):77-80.
[9]陈 超,梁 卓,李小燕,等.生态修复在景观水体治理中的应用[J].安徽农学通报,2010,16(1):136-138,179.
[10]胡振华,解明曙,王治国.晋西黄土残塬区水土保持生态建设模式探讨[J].水土保持研究,2003(2):126-130.
[11]温东辉,唐孝炎,马倩茹.天然沸石铵吸附容量研究[J].安全与环境工程,2003,16(2):31-34.
[12]朱 俊,王 宁.天然沸石在环保中的应用[J].矿物学报,2003,23(3):250-254.
[13]张宁克,魏 薇.吉林省沸石的性质与应用[J].吉林地质,2004(3):72-81.
