多黏菌素E注射制剂及其临床应用
2013-04-04陈玉双郑玉林管海英黄君勤
陈玉双 郑玉林 管海英 黄君勤
(上海新亚药业有限公司 上海 201203)
多黏菌素E(polymyxin E)是由1950年小山康夫在日本福岛县分离出的多黏芽胞杆菌变种(Bacillus polymyxa var. colistimus)的发酵培养液中提取的一种碱性多肽类抗生素,对革兰阴性杆菌有强烈的抑菌作用[1]。因为肾毒性和神经毒性,多黏菌素E在20世纪70年代逐渐被其他毒性低、疗效好的抗生素所取代。近年来,随着多药耐药(multidrug resistance, MDR)革兰阴性杆菌的出现,包括铜绿假单胞菌、鲍氏不动杆菌和肺炎克雷伯菌等引起的感染已经成为严重的临床问题。在新药开发有限的情况下,多黏菌素E又重新焕发了青春,在多药耐药菌的治疗方面获得了越来越多的应用[2]。由于上市较早,多黏菌素E产品在各国均未经过严格的新药开发流程监控,早期的药动学、药效学、毒理学等资料非常有限,缺少指导临床使用的相关信息。由此造成的用药不合理,已导致了对多黏菌素类耐药的细菌出现[3]。近期,很多学者逐渐开始关注这一药物的基础研究工作,相关的报道正在日益增多。为了更好的指导临床用药以及避免药物的滥用,本文对多黏菌素E产品信息以及临床应用进行了综述。
1 理化性质
多黏菌素E又名黏杆菌素、黏菌素、克利斯汀、抗敌素等,它是一种多组分的白色结晶或结晶性粉末混和物,主要成份为多黏菌素E1(C53H100N16O13)和多黏菌素E2(C53H98N16O13)。不同的原料供应商和不同批次之间,上述两种主要成分的比例是不同的。多黏菌素E是由七环和末端的三肽组成的十肽菌素,尾部的脂肪酸通过酰胺键连接到末端的三肽,七环有亲水端和疏水端,三肽只有亲水端。
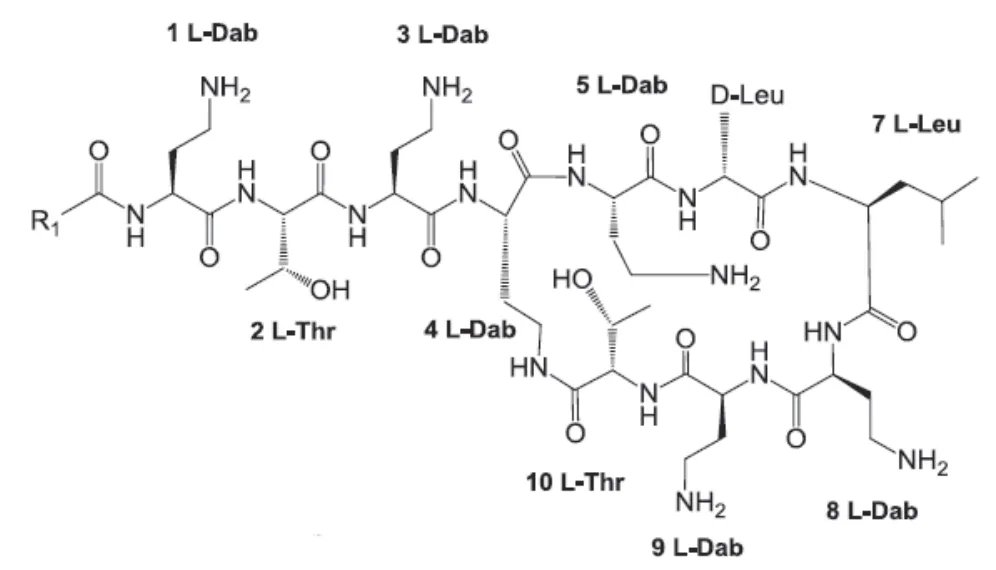
图1 多黏菌素E分子结构[4]
目前有两种形式的多黏菌素E可供使用:硫酸多黏菌素E(colistin sulphate)与多黏菌素甲磺酸钠(colistimethate sodium,CMS)。CMS是多黏菌素E与甲醛和亚硫酸氢钠的反应产物。因此,硫酸多黏菌素E与CMS有着不同的结构,并不是多黏菌素E的不同盐,CMS为多黏菌素E的非活性前体药物。在生理pH条件下,硫酸多黏菌素E为聚阴离子,CMS为聚阳离子。实验表明,多黏菌素E抗铜绿假单胞菌的活性为CMS的三倍。在水溶液中,CMS自动水解形成活性成分多黏菌素E。患者静脉注射CMS之后转化成多黏菌素E,后者在体内进行循环[5]。
2 作用机制和耐药性
尽管已经面世超过半个世纪,人们对于多黏菌素E抗菌活性其作用机制尚未有清晰的解释。当前,人们倾向于认为,既然多黏菌素E和多黏菌素B的化学结构仅相差一个氨基酸,二者的作用机制也应该相同。多黏菌素E抗菌活性的主要靶点是革兰阴性细胞壁上的脂多糖。多黏菌素E结构中氨基酸的正电荷以及肽环与脂多糖有着高度的亲和性。多黏菌素E通过与脂多糖分子的相互静电作用以及二价阳离子(Ca2+和Mg2+)的竞争性置换,破坏膜的通透性,使细胞内的主要成份流出,进而导致细胞死亡。多黏菌素E诱导细菌死亡的精确机制尚未研究清楚,可能会涉及到多种细菌细胞靶点。多黏菌素E也会与脂多糖上面的磷脂A部分结合,在动物实验中阻碍多种内毒素的生物效应[6]。
当前多黏菌素E的耐药性较为少见,很可能是因为过去的几十年内使用较少的原因。近十年来,随着使用多黏菌素E治疗MDR的应用增加,已经出现了对多黏菌素E耐药细菌的报道。目前,人们识别出的多黏菌素E耐药细菌包括大肠杆菌、伤寒沙门菌、克雷伯氏菌、铜绿假单胞菌、鲍氏不动杆菌等[3,7]。其中,克雷伯氏菌和铜绿假单胞菌出现了异质性耐药。根据当前的研究,多黏菌素E的耐药机制主要是多黏菌素E作用的起始位点细菌LPS的改良,其他的耐药机制包括外膜的改变以及钾离子外流系统等。一项近期的多黏菌素E耐药细菌风险因素研究显示,CMS和硫酸多黏菌素E的使用是唯一的独立风险因素[8]。该项研究提示我们,多黏菌素E的广泛长期使用可能会导致多黏菌素E耐药菌株的泛滥,所以应该避免不必要的或者长期的多黏菌素E治疗。
3 处方、剂量和给药途径
CMS的给药途径包括非肠道给药、静脉给药、肌内给药、吸入给药。CMS在国际上应用广泛,包括北美、南美、澳大利亚、欧洲、亚洲等多个地区和国家均有应用。硫酸多黏菌素E的给药途径包括非肠道给药、静脉给药、肌内给药、吸入给药、口服(肠道消毒,无吸收)和外用(用于细菌性皮肤感染的治疗)。静脉给药的硫酸多黏菌素E仅在中国批准应用。肌内给药的形式局部疼痛较为显著并且个体吸收差异较大,目前已经很少在临床上使用。
当前市售可用的多黏菌素E注射配方主要有三种,欧美范围内主要为两种CMS配方[9]。其中一种为欧洲上市销售的colomycin injection 制造商Alpharma A/S,Copenhagen, Denmark (now Actavis Group, Iceland),分销商Forest Laboratories, Kent, United Kingdom。每瓶中包含0.5x106、1x106或者2x106国际单位(IU)的CMS。根据药物国际单位的定义,pH 7.2条件下1 ml肉汤中可以抑制大肠杆菌95 ISM生长的多黏菌素E的量定义为1 IU。根据此定义推算,纯多黏菌素E每毫克效价为30 000 IU,CMS每毫克效价为12 500 IU。2x106IU相当于160 mg CMS。另一种为美国市场销售的Coly-Mycin M Parenteral,制造商Parkedale Pharmaceuticals,Inc., Rochester, Mich.,分销商Monarch Pharmaceuticals,Inc., Bristol, Tenn。以多黏菌素E计,规格为150 mg/瓶,相当于360 mg的CMS或者是4.5x106IU的CMS。CMS用于成人全身感染的剂量范围在240~720 mg/d[(3~9)×106IU/d],每天应用2~4次。中国上市销售的产品为硫酸多黏菌素E,商品名为可利斯安,规格为0.5×106IU。硫酸多黏菌素E的成人全身感染的剂量范围在(1~1.5)×106IU/d,每天应用2~3次。
3.1 静脉注射给药
Kapoor等[10]报道,50例MDR革兰阴性杆菌感染的危重患儿,病原菌是鲍曼不动杆菌、铜绿假单胞菌、肺炎克雷伯菌、大肠杆菌、阴沟肠杆菌。患儿接受静脉注射多黏菌素治疗后,36例(72%)出现较好的治疗效果,14例死于伴有多器官功能障碍综合征的脓血症。5例出现肾毒性的患儿中,3例是由于多器官功能障碍综合征,2例同时使用了万古霉素。未有由多黏菌素治疗引发的神经毒不良反应报道。作者认为静脉注射多黏菌素对于儿童MDR革兰阴性杆菌感染的治疗有作用,但是其在儿童中的安全性和疗效仍需要进一步确证。
相关的临床报道还有很多,此处不再一一枚举。需要指出的有以下几点:①当前的临床研究尚存在一些局限性,包括患者数量少、无对照组、结果定义差异等,在此后的研究中仍需要加以改善。②当前的研究通常是CMS和其他抗生素的联合用药,缺乏CMS单独给药和联合用药效果的对比性研究。仍需要开展目标人群的具有良好试验设计的随机对照试验,用以考察CMS的确切疗效。③CMS是多黏菌素E的前体药物,其在体内的PK/PD(药代动力学/药效学)数据尚需要深入的研究。在治疗相应疾病的过程中,多黏菌素E的起效浓度、使用剂量的CMS转化为多黏菌素E的比例和速度、以及是否有更好的给药方案仍旧需要深入的研究,以便临床医师能够能准确的应用CMS。④我国作为全球唯一批准硫酸多黏菌素E静脉注射给药的国家,目前尚未查到关于临床使用注射用硫酸多黏菌素E的相关报道(无论是不良反应还是临床效果),这方面的工作还需要各方齐心协力深入研究。
3.2 雾化吸入给药
尽管CMS的吸入给药并未经过FDA的批准,但是此种给药途径在全球范围内的囊肿性纤维化(CF)诊所以及重症监护病房都有应用[11]。近年来使用CMS吸入治疗报道的增加主要是因为MDR革兰氏阴性菌感染造成的呼吸机相关肺炎日益增加。尽管目前的研究对多黏菌素E的吸入应用做出了正面的评价,仍旧有几个因素是该种给药途径的制约因素:首先,该种给药途径并未经过任何国家的审批,存在法规性风险。其次,没有合适的药物制剂可供使用。用于肺部吸入式给药的溶液一般是冻干注射用制剂重建后或是医院药剂科或其他供应商自制的专门用于吸入的溶液。最后,吸入给药的浓度、剂量等参数没有给定的标准。上述各种因素综合在一起给有可能会给临床医师的用药带来意想不到的麻烦。最近,1例CF患者因为吸入CMS造成了死亡,FDA给出了警告[12]。这一事件也给希望应用CMS的吸入给药的临床医师敲响了警钟。
3.3 鞘内或脑室内给药
多黏菌素E穿透血脑屏障的透过率约为5%,在炎症等情况下最高可达到25%~67%。静脉注射给药无效或者因为血脑屏障等因素造成CMS无法到达感染部位的情况下,可以考虑使用鞘内或脑室内给药途径。CMS的鞘内或脑室内给药治疗中枢神经系统感染的报道和综述已有多篇[13-14]。尽管同时出现了化学性脑室炎等不良反应,但是考虑到此种治疗方式所达到的疗效和安全性,此种治疗方式仍有进一步研究和应用的价值。
3.4 膀胱灌注治疗
近期的一篇报道[15]显示,一例肿瘤切除术后的患者在接受替加环素和CMS长期治疗后,仍存在多药耐药的鲍曼不动杆菌引起的持续尿路感染。患者接受CMS膀胱灌注治疗,数天后治愈,并未出现任何不良反应。此种治疗方式对于MDR革兰阴性菌造成的尿路感染患者可能是很好的选择。
4 不良反应
多黏菌素E静脉注射给药后最常见的毒性反应是肾毒性。一项近期开展的前瞻性对比研究显示,在研究结束时多黏菌素E更易于导致肾毒性,其毒性高于β-内酰胺类抗生素[16]。研究显示多黏菌素E肾毒性的风险因素包括高龄、已存在的肾功能不全、低白蛋白血症、同时使用非甾体抗炎药或者万古霉素等[17]。总体而言,当前报道的肾毒性发生率低于以往的研究。毒性降低的可能因素包括化合物纯度提高、重症监护病房监控的改善以及避免同时使用其他肾毒性药物等。关于多黏菌素E的肾毒性,我们尤其需要关注的是,多黏菌素E是用于治疗威胁生命安全的多药耐药革兰阴性杆菌所引起的感染,在考虑肾毒性损害时需要对该产品的风险收益比率进行综合的考量。
神经毒性的发生率要低于肾毒性。临床症状包括头晕、肌无力、感觉异常、听力部分丧失、视力障碍、眩晕、意识混乱、幻觉、抽搐、共济失调、神经肌肉阻滞等。感觉异常是最常见的临床表现,约27%的病例使用静脉注射甲磺酸黏菌素钠报告。神经毒性通常是较温和的,在停药之后即可恢复[18]。
5 总结
当前,人们对于多黏菌素E的了解仍旧是以20世纪70年代以前的研究结果为主。尽管近年来该产品在临床方面的使用逐渐增加,但是理论方面的研究仍旧不足。首先,几种上市销售的产品在剂量标识和定义等方面需要统一,国际单位、多黏菌素E、CMS等不同的表述方式给相关的研究带来很多理解上的误区,医师和研究人员在阅读相关文献时很容易对使用的剂量造成误解。其次,因为PK/PD数据的缺乏,在确定给药剂量方面,临床医师很难做出正确的选择。面对当前MDR的泛滥,作为“最后的防线”的多黏菌素E很容易会出现滥用,进而造成多黏菌素E耐药菌株的大量出现。在此种情况下,更要加强基础研究以及对临床医师的指导,严格控制多黏菌素E的应用范围。最后,鉴于当前多黏菌素E品种的匮乏,以及该产品本身的不良反应,有必要进一步开发各种新剂型,同时起到降低不良反应和提高疗效的作用。
[1] Velkov T, Roberts KD, Nation RL,et al. Pharmacology of polymyxins: new insights into an ‘old’ class of antibiotics[J].Future Microbiol, 2013,8(6): 711-724.
[2] Michalopoulos AS, Karatza DC. Multidrug-resistant Gramnegative infections: the use of colistin[J]. Expert Rev Anti Infect Ther, 2010,8(9): 1009-1017.
[3] Oostdijk EA, Smits L, de Smet AM,et al. Colistin resistance in gram-negative bacteria during prophylactic topical colistin use in intensive care units[J]. Intensive Care Med, 2013,39(4): 653-660.
[4] Bergen PJ, Landersdorfer CB, ZhangJ, et al.Pharmacokinetics and pharmacodynamics of ‘old’polymyxins: what is new[J]. Diagn Microbiol Infect Dis,2012, 74(3) :213-223.
[5] Boisson M, Gregoire N, Couet W,et al. Colistin in critically ill patients[J]. Minerva Anestesiol, 2013,79(2): 200-208.
[6] Lim LM, Ly N, Anderson D,et al. Resurgence of colistin:a review of resistance, toxicity, pharmacodynamics, and dosing[J]. Pharmacotherapy, 2010,30(12): 1279-1291.
[7] Apisaranthanarak A, Rujanavech S, Luxamesathaporn P,et al. Intensified infection control measures to minimize the spread of colistin-resistantAcinetobacter baumannii[J]. Infect Control Hosp Epidemiol, 2013,34(4): 445-447.
[8] Matthaiou DK, Michalopoulos A, Rafailidis PIet al. Risk factors associated with the isolation of colistin-resistant gramnegative bacteria: a matched case-control study[J]. Crit Care Med, 2008, 36(3): 807–811.
[9] Yahav D, Farbman L, Leibovici L,et al. Colistin: new lessons on an old antibiotic[J]. Clin Microbiol Infect, 2012,18(1): 18-29.
[10] Kapoor K, Jajoo M, Dublish S,et al. Intravenous colistin for multidrug-resistant gram-negative infections in critically ill pediatric patients[J]. Pediatr Crit Care Med, 2013, Epub ahead of print.
[11] Maiz L, Giron RM, Olveira C,et al. Inhaled antibiotics for the treatment of chronic bronchopulmonaryPseudomonas aeruginosainfection in cystic fibrosis: systematic review of randomised controlled trials[J]. Expert Opin Pharmacother,2013,14(9): 1135-1149.
[12] Colistimethate (marketed as Coly-Mycin M and generic products) Information[EB/OL]. [2009-05-13]. http: //www.fda.gov/Drugs/DrugSafety/PostmarketDrugSafetyInformation forPatientsandProviders/ucm118080.htm.
[13] Karaiskos I, Galani L, Baziaka F,et al. Successful treatment of extensively drug-resistantAcinetobacter baumanniiventriculitis and meningitis with intraventricular colistin after application of a loading dose: a case series[J]. Int J Antimicrob Agents, 2013,41(5): 480-483.
[14] Karaiskos I, Galani L, Baziaka F,et al. Intraventricular and intrathecal colistin as the last therapeutic resort for the treatment of multidrug-resistant and extensively drug-resistantAcinetobacter baumanniiventriculitis and meningitis: a literature review[J]. Int J Antimicrob Agents, 2013,41(6):499-508.
[15] Volkow-Fernandez P, Rodriguez CF, Cornejo-Juarez P.Intravesical colistin irrigation to treat multidrug-resistantAcinetobacter baumanniiurinary tract infection: a case report[J]. J Med Case Rep, 2012,6(1): 426.
[16] Paul M, Bishara J, Levcovich A,et al. Effectiveness and safety of colistin: prospective comparative cohort study[J]. J Antimicrob Chemother, 2010,65(5): 1019-1027.
[17] Rattanaumpawan P, Ungprasert P, Thamlikitkul V. Risk factors for colistin-associated nephrotoxicity[J]. J Infect,2011,62(2): 187-190.
[18] Falagas ME, Rafailidis PI. Nephrotoxicity of colistin: new insight into an old antibiotic[J]. Clin Infect Dis, 2009, 48(12):1729-1731.
