载肝素钠ACA微胶囊载药量
2012-12-29龙瑞敏王曦蓝琪王士斌
龙瑞敏,王曦,蓝琪,王士斌,2
(1.华侨大学 化工学院,福建 厦门 361021;2.华侨大学 生物材料与组织工程研究所,福建 厦门 361021)
载肝素钠ACA微胶囊载药量
龙瑞敏1,王曦1,蓝琪1,王士斌1,2
(1.华侨大学 化工学院,福建 厦门 361021;2.华侨大学 生物材料与组织工程研究所,福建 厦门 361021)
采用乳化固化法制备粒径为820nm的海藻酸钙微球,同时采用两步成囊的方法在微球表面包覆几丁聚糖半透膜并制备海藻酸钙/几丁聚糖微胶囊.以肝素为模型药物,考察微球溶胀与非溶胀、加药浓度、载药方式、几丁聚糖相对分子质量、成膜时间、成膜液浓度、几丁聚糖改性物等因素对载药的影响.研究结果表明:所制备的微胶囊载药量最高可达77.4%.
海藻酸钠;几丁聚糖;微胶囊;肝素;载药量
海藻酸钠-壳聚糖-海藻酸钠(ACA)微胶囊是目前研究较为广泛的药物缓、控释制剂之一[1-2],主要是因为其采用了天然的藻酸盐和几丁聚糖材料.海藻酸钠是从褐藻中提取的一类天然多糖,在生理条件下可与聚阳离子或两性大分子电解质交联而形成聚电解质复合囊材;几丁聚糖是天然多糖中唯一的碱性多糖,来源丰富,无毒,易化学修饰,具有良好的生物相容性和可生物降解性.低分子肝素(LMWH)是一类抗血栓活性药物,由肝素分解或降解得到的阴离子低聚物,临床上主要用于血液透析的抗凝治疗及防治各种血栓、栓塞等[3-4].肝素作为抗凝血药物的使用受到诸多限制,主要是其在体内不稳定及用药时的副作用.将LMWH制成适用于静脉注射或栓塞的缓释型制剂,可保持肝素的活性,提高LMWH的疗效,降低其毒副作用[5-6].然而近年来,随着人们对蛋白/多肽类药物的缓、控释制剂的研究表明,制备过程中存在稳定性差、载药量低,以及体内外突释效应明显等问题[7-8],其中载药量是涉及到实际应用的一个关键指标.为了制备载药量理想的微胶囊,本课题组在前期研究中制备了载药量高达64.8%的海藻酸钙/聚组氨酸微胶囊[9],以及载药量为44.29%的海藻酸钙/几丁聚糖微胶囊[10].影响载药量的因素除了上述文献报道的药物的初始浓度、成膜材料的浓度与相对分子质量之外,在其过程当中的诸多因素也可能影响到载药量的大小,如微球是否溶胀、载药方式(静/动态)、成膜时间、膜材的选择(几丁聚糖改性物)等 .本文在此基础上进一步探讨各种因素对微胶囊载药性能的影响,制备出粒径较小、分布均匀、球形度好的高载药海藻酸钙/几丁聚糖微胶囊.
1 材料与方法
1.1 试剂与仪器
1)试剂.几丁聚糖(平均相对分子质量为50 000,100 000,150 000,浙江金壳生物化学有限公司);海藻酸钠(化学纯,上海国药集团化学试剂有限公司);肝素钠(≥150IU·mg-1,上海楷洋生物技术有限公司);Span 80和Tween 80为化学纯,其他试剂均为分析纯(广东汕头市西陇化工厂).
2)仪器.BS210S型电子分析天平(德国Sartorius公司);SP-2102U型紫外可见分光光度计(上海光谱仪器有限公司);FDU-2100型冷冻干燥仪(日本东京理化器械株式会社);Winner 2000型激光粒度分析仪(济南微纳仪器有限公司);RW20DZM.n型数显电动搅拌机(德国IKA公司);S-3500N型扫描电子显微镜(日本HITACHI公司);LD4-2型低速离心机(北京医用离心机厂).
1.2 海藻酸钙微球的制备
分别取质量浓度为10g·L-1的海藻酸钠溶液和40g·L-1Span 80异辛烷溶液,混合后,于高速电动搅拌机上以1 500r·min-1搅拌10min,形成油包水(W/O)型体系;然后加入一定量的Tween 80溶液,继续搅拌乳化5min,于500r·min-1下缓慢滴加一定量的8.0%的氯化钙溶液,再搅拌固化10 min,加入10mL无水乙醇静置分层.以3 000r·min-1离心分离出海藻酸钙微球,依次用体积分数为40%,60%,80%,100%的乙醇进行梯度洗脱,最后将所得微球置于37℃,-0.1MPa真空干燥箱中干燥过夜.
1.3 海藻酸钙/几丁聚糖载药纳米微胶囊的制备
取30mg干燥的空白海藻酸钙微球,用蒸馏水溶胀30min后,分散悬浮于肝素钠溶液中,载药24 h;离心去上清液,加入10mL一定浓度的几丁聚糖溶液,用漩涡振荡仪振荡成膜10min,接着离心去除上清液,再用pH值为7.4磷酸盐缓冲液(PBS)洗涤一次,于-20℃预冻;放入冷冻干燥机中冻干,24h后取出,即制得载药纳米微胶囊.
1.4 微球的性能
1.4.1 形态特征与粒径分布 通过扫描电镜观察微球形貌,并以蒸馏水为流动相,用激光粒度分析仪来测定微球的粒径分布.
1.4.2 载药量[11]称取适量的载药微胶囊,分散于20mL破囊液[12]中,待破囊后,用分光光度法在258.0nm检测肝素钠含量,每组数据取3个平行样的平均值,计算微囊的载药量.载药量(Q)是指微球中所含药物的量.
2 结果与讨论
2.1 微球的形态与粒径分布
采用优化后的制备条件:海藻酸钠质量浓度为10g·L-1,氯化钙质量浓度为80g·L-1,亲水亲油平衡值(HLB)为6.0,乳化搅拌速度1 500r·min-1,乳化时间为15min,油水相比例为1∶1,固化搅拌速度为500r·min-1,固化时间为10min.所得到的微球的形态与粒径分布,分别如图1,2所示 .图2中:φ为粒径;F为分布比例 .由图1,2可知:微球表面光滑、球形度好,微球分散性好,粒径较小,粒径集中分布在0.47~1.02μm,平均粒径为0.82μm.

图1 微球的SEM图Fig.1 SEM picture of microspheres
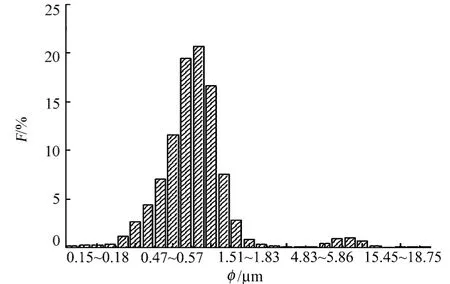
图2 微球的粒径分布图Fig.2 Particle size distribution of microspheres
2.2 微球溶胀与非溶胀对载药量的影响
微球溶胀与非溶胀对载药量(Q)的影响,如图3所示.由图3可以知道:溶胀微球的平均载药量为50.8%,非溶胀的微球平均载药量为27.5%,说明微球经过溶胀后,载药量明显变大,载药效果好.究其原因是由于微球溶胀后,海藻酸钙凝胶珠网孔孔径会变大,从而导致吸附载药时,药物容易扩散进去海藻酸钙凝胶网络内部,载入的绝对药量增大,微囊载药量相应就变大;而未经溶胀的微球,网孔的孔径较小,吸附进入海藻酸钙微胶囊内部的药物相对较少,所以载药量相对低.
2.3 初始载药浓度对载药量的影响
破囊法和上清液法在不同初始药物浓度(c0)时对载药量(Q)的影响,如图4所示.由图4可知:破囊法的结果要明显高于上清液法.当载药液浓度分别为0.5,1.0,2.0mol·L-1时,破囊法的平均载药量分别为40.1%,46.9%,47.6%.随着肝素钠浓度增大,载药量增加.分析认为,随着投药浓度的增大,单位体积内含有的肝素钠更多,同等情况下,扩散进入海藻酸钙凝胶网络内部载入的绝对药量也会相应增大.孙学战等[10]研究了BSA载药时的情况,取得了一致的结果,也进一步证明了载药时药物主要依靠空白微球内部与药液之间存在的浓度梯度完成向微球内部的扩散,载药浓度越大,这种浓度梯度就越大,越有利于药物向微球内部扩散.
对比上清液法和破囊法两种测微囊载药量的方法,由于上清液法在载入肝素钠的微球成膜前测吸光度值,同时由于上清液中可能掺杂部分微球成分造成干扰,使测定数值严重失真,因此破囊法更接近实际情况,也是各项测定中实际采用的方法.
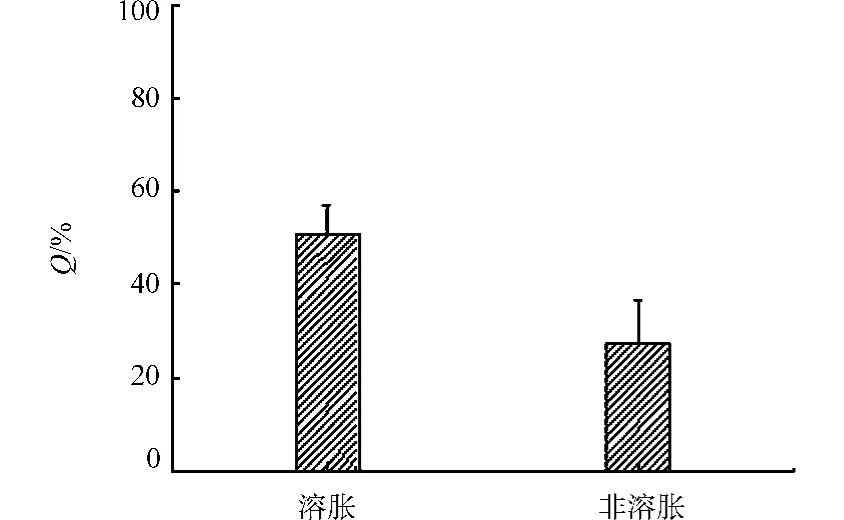
图3 微球溶胀与非溶胀对微囊载药量的影响Fig.3 Influence of swelling/non-swelling on microcapsule drug-loading
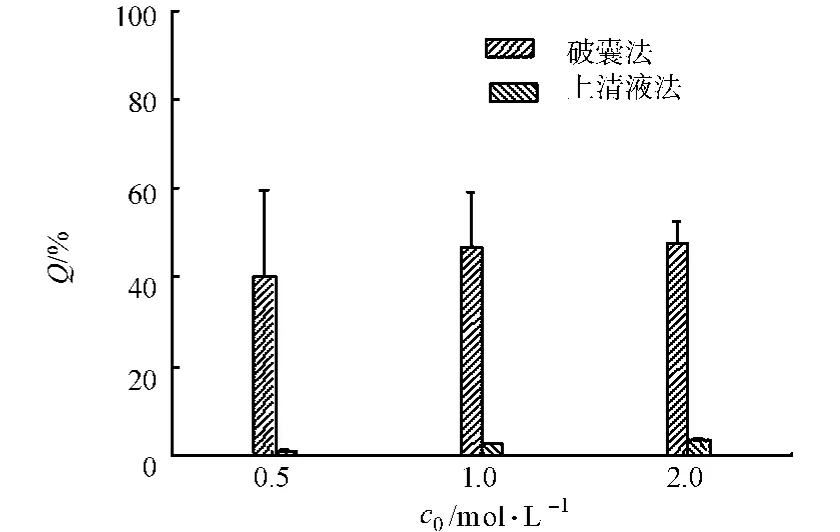
图4 载药浓度对微囊载药量的影响Fig.4 Influence of initial drug concentration on microcapsule drug-loading
2.4 载药方式对载药量的影响
载药方式对载药量(Q)的影响,如图5所示.由图5可知:在4℃冰箱、37℃水浴槽、37℃摇床载药条件下,平均载药量分别为35.1%,39.8%,47.2%.通过比较可以看出:在37℃摇床条件下,载药量是最大的.这主要由于摇床状态下的对流扩散的物质传递速率要大于静止状态下的只有分子扩散时的速率,而且随温度的升高,肝素钠分子运动越激烈,所以37℃比4℃条件下的载药量也要高些.
在实验中也发现:37℃水浴槽和37℃摇床条件下的微囊产量相对较少,这可能是由于在37℃时,温度相对较高,微囊溶胀程度更大,海藻酸钙与几丁聚糖的交联相对不稳定,成膜后用PBS洗涤时,容易破碎,导致产量降低.稳定性实验也表明:4℃时肝素钠具有较强的稳定性,利于后续的载药及释放.

图5 载药方式对微囊载药量的影响Fig.5 Influence of drug-loading condition on microcapsule drug-loading
2.5 几丁聚糖相对分子质量对载药量的影响
几丁聚糖相对分子质量(Mr)对载药量(Q)的影响,如图6所示.由图6可以知道:当几丁聚糖相对分子质量为50 000,100 000,150 000时,平均载药量分别为52.4%,39.3%,20.8%.随着几丁聚糖相对分子质量的增加,微囊的载药量有所下降,显示出低相对分子质量的几丁聚糖有相对较高的载药量.可能的原因是,相对分子质量较大的几丁聚糖具有更多的结合位点,与海藻酸钙结合而成的膜更致密,几丁聚糖占据了海藻酸钙胶珠较大的空间,而将药物分子挤出;同时,几丁聚糖相对分子质量越大,微囊就越重,从而减少了药物在微囊中的质量分数,导致载药量的下降.Wang等[13]对聚精氨酸微胶囊的研究也表明:高分子膜材相对分子质量越低,形成的微胶囊膜越厚,膨胀率也越大.这样就扩大了微胶囊的内部空间,且载入的药物也不易漏出,从而增大了药物的载入量.
2.6 成膜时间对载药量的影响
成膜时间(t)对载药量(Q)的影响,如图7所示.由图7可知:成膜时间为5,10,15min时,平均载药量分别为31.7%,48.2%,39.3%;随成膜时间延长,平均载药量有一个先增后减的趋势.由于载药过程是一个动态平衡,当成膜时间逐步增大到10min时,随着成膜时间增加,几丁聚糖与海藻酸钙分子结合的膜更充分更紧密,使药物肝素钠不易扩散出几丁聚糖-海藻酸钙膜,导致载药量增大.当成膜时间增大到15min时,由于几丁聚糖与海藻酸钙反应已达平衡,药物会因为扩散作用向外泄漏导致载药量降低.刘源岗等[14]考察了成膜反应时间与膜强度的关系,表明随着成膜反应时间的延长,膨胀率降低,膜强度提高,其中膨胀率的变化初期(≤10min)下降快,并随着时间增长下降减慢.这一变化规律与文中结果也是基本一致的.

图6 几丁聚糖相对分子质量对微囊载药量的影响Fig.6 Influence of chitosan molecular weight on microcapsule drug-loading

图7 成膜时间对载药量的影响Fig.7 Influence of membrane forming time on microcapsule drug-loading
2.7 几丁聚糖浓度对载药量的影响
几丁聚糖浓度(c(几丁聚糖))对载药量(Q)的影响,如图8所示.通过图8可以看出:在几丁聚糖浓度为0.1,0.2,0.5mol·L-1下,微囊的平均载药量分别为43.6%,56.9%,77.4%;随着几丁聚糖浓度的增大,微胶囊的载药量也随之增大.究其原因可能是钙离子与海藻酸钠中的古罗糖醛酸残基结合形成一种多孔性的网状结构,通常称为“egg-box”结构;而几丁聚糖通过静电作用可以在其表面复合形成聚电解质半透膜,一方面增加了微球对药物的吸附包裹能力,另一方面也限制了药物向外扩散,减少了药物的损失从而提高了载药量.此外,文献[15]的研究也表明,微囊的载药量随着几丁聚糖浓度增加而增加是有一定范围的,超过这个浓度范围,载药量不仅不会增加,反而会有所下降.
2.8 改性几丁聚糖对载药量的影响
羧化几丁聚糖、几丁聚糖盐酸盐、固体类透明质酸几丁聚糖等3种改性几丁聚糖对微胶囊载药性能的影响,如图9所示.由图9可以看出:羧化几丁聚糖、几丁聚糖盐酸盐、固体类透明质酸几丁聚糖的平均载药量分别为74.4%,17.9%,19.4%,表明羧化几丁聚糖做为膜材时,载药效果最好.

图8 几丁聚糖浓度对载药量的影响Fig.8 Influence of chitosan concentration on microcapsule drug-loading

图9 改性几丁聚糖对载药量的影响Fig.9 Influence of modified chitosan on microcapsule drug-loading
3 结束语
采用乳化固化法制备的海藻酸钙微球,具有粒径较小、分布均匀、球形度好的特点 .采用两步成囊的方法在微球表面包覆几丁聚糖半透膜制备了海藻酸钙/几丁聚糖微胶囊,考察了不同因素对微胶囊载药性能的影响,制备的微胶囊载药量最高可达77.4%,为该型载体应用于蛋白、多肽类药物的缓/控释的实际应用提供了可参考的实验依据.
[1]刘袖洞,于炜婷,王为,等.海藻酸钠和壳聚糖聚电解质微胶囊及其生物医学应用[J].化学进展,2008,20(1):126-139.
[2]YU Wei-ting,SONG Hui-yi,ZHENG Guo-shuang,et al.Study on membrane characteristics of alginate-chitosan microcapsule with cell growth[J].Journal of Membrane Science,2011,377(1/2):214-220.
[3]YOUNG E.The anti-inflammatory effects of heparin and related compounds[J].Thrombosis Research,2008,122(6):743-752.
[4]AUGOUSTIDES J G T.Update in hematology:Heparin-induced thrombocytopenia and bivalirudin[J].Journal of Cardiothoracic and Vascular Anesthesia,2011,25(2):371-375.
[5]牟善松,屠美,丁珊,等.不同材料包裹的肝素缓释微囊生物相容性评价[J].材料导报,2003,17(5):79-81.
[6]LI Li,BAE B C,TRAN T H,et al.Self-quenchable biofunctional nanoparticles of heparin-folate-photosensitizer conjugates for photodynamic therapy[J].Carbohydrate Polymers,2011,86(2):708-715.
[7]王襄平,梅兴国.多肽及蛋白类药物微球包封率和释放的研究进展[J].国外医学药学分册,2006,33(3):219-223.
[8]王丹.多肽及蛋白类药物微球的载体材料、制备以及突释现象[J].中国组织工程研究与临床康复,2008,12(10):1931-1934.
[9]吴文果,黄晓楠,王士斌,等.乳化法制备海藻酸钙/聚组氨酸微胶囊[J].化工进展,2009,28(4):673-677.
[10]孙学战,刘源岗,王士斌,等.高载药量海藻酸钙/几丁聚糖微胶囊的性能[J].化工进展,2010,29(9):1725-1729.
[11]国家药典委员会.中华人民共和国药典[M].北京:化学工业出版社,2005.
[12]薛伟明,于炜婷,刘袖洞,等.载细胞海藻酸钠/壳聚糖微胶囊的化学破囊方法研究[J].高等学校化学学报,2004,25(7):1342-1346.
[13]WANG Shi-bin,LIU Yuan-gang,WENG Lian-jin,et al.Effect of the molecular weights of poly-L-arginine on membrane strength and permeability of poly-L-arginine group microcapsules[J].Macromolecular Bioscience,2003,3(7):347-350.
[14]刘源岗,王士斌,王莹.海藻酸钙-聚精氨酸聚电解质微胶囊强度性能研究[J].功能材料,2009,40(1):119-122.
[15]舒晓正,朱康杰.壳聚糖-海藻酸钠微囊对蛋白质控制释放的研究[J].功能高分子学报,1999,12(4):423-426.
Study of the Drug-Loading Property of Heparin-Loading ACA Microcapsules
LONG Rui-min1,WANG Xi1,LAN Qi1,WANG Shi-bin1,2
(1.College of Chemical Engineering,Huaqiao University,Xiamen 361021,China;2.Institute of Biomaterials and Tissue Engineering,Huaqiao University,Xiamen 361021,China)
Calcium alginate microspheres with mean diameter 820nm and calcium alginate/chitosan microcapsules were prepared by emulsion-curing.Using heparin as a model drug,the effects of the swelling condition,the different concentrations of heparin,the drug-loading condition,chitosan molecular weight,the membrane forming time,the different concentrations of chitosan and different modified chitosans on drug-loading were investigated.Results indicated that the maximum drug-loading was 77.4%.
alginate;chitosan;microcapsule;heparin;drug-loading
R 318
A
1000-5013(2012)03-0285-05
2011-09-29
龙瑞敏(1979-),女,实验师,主要从事材料的开发与应用的研究.E-mail:simplever@126.com.
国家863计划基金资助项目(2006AA02A118);国家自然科学基金资助项目(31000441);中央高校基本科研业务费专项基金资助项目(JB-SJ1009;JB-JC1009);华侨大学科研基金资助项目(10HZR10)
(责任编辑:钱筠 英文审校:刘源岗)
