硝酸钠与十二烷基苯磺酸钠在二氧化氯介质中对铝合金的协同缓蚀作用研究
2012-12-26王奎涛高金龙吴海霞李文亚
王奎涛,鲁 楠,高金龙,吴海霞,李文亚
(1.河北科技大学化学与制药工程学院,河北石家庄 050018;2.河北科技大学河北省药物化工工程技术研究中心,河北石家庄 050018)
硝酸钠与十二烷基苯磺酸钠在二氧化氯介质中对铝合金的协同缓蚀作用研究
王奎涛1,2,鲁 楠1,2,高金龙1,2,吴海霞1,2,李文亚1,2
(1.河北科技大学化学与制药工程学院,河北石家庄 050018;2.河北科技大学河北省药物化工工程技术研究中心,河北石家庄 050018)
为了探讨二氧化氯(ClO2)介质中金属的腐蚀问题,采用静态失重法、动电位极化曲线法和扫描电镜法研究了硝酸钠和十二烷基苯磺酸钠(DBSAS)在100mg/L二氧化氯介质中对铝合金的缓蚀协同效应。结果表明,硝酸钠对铝合金的缓蚀作用较差,最大缓蚀率仅为55.58%;DBSAS对铝合金有中等程度的缓蚀作用,缓蚀效率随其浓度的增加而增大,最大缓蚀率可达89.33%;硝酸钠和DBSAS复配后对铝合金产生明显的缓蚀协同效应,当硝酸钠和DBSAS复配的质量之比为3∶7时,最大缓蚀率可达96.28%。
二氧化氯;铝合金;硝酸钠;十二烷基苯磺酸钠;缓蚀剂;协同作用
二氧化氯(ClO2)是世界卫生组织确认的第4代A1级安全消毒剂,与其他消毒剂相比,它不仅能分解残留的细菌组织,还不会产生三氯甲烷等致癌物质。目前,二氧化氯产品已在医疗器械、日常生活中的清洁消毒中得到推广与关注[1-4]。但是,二氧化氯水溶液具有一定的氧化性及弱酸性,在高浓度下,会对金属器具造成一定程度的腐蚀[5]。因此,针对二氧化氯体系进行的防腐蚀研究备受关注。普通缓蚀剂在酸性条件下无法抵抗二氧化氯的强氧化性[6-7],起不到缓蚀作用。本实验以此为切入点,研究铝合金在二氧化氯应用的极限浓度中的腐蚀情况,并探讨硝酸钠与十二烷基苯磺酸钠(DBSAS)在该体系中对铝合金的缓蚀协同性能,寻找适用于二氧化氯体系中的铝合金缓蚀剂。
1 实验部分
1.1 仪器与试剂
分析天平(AL204,梅特勒-托利多公司提供);二氧化氯检测仪(DR/890,美国哈希公司提供);电化学工作站(CHI660B,上海辰华仪器公司提供);数控超级低温恒温槽(SDC-6,宁波天恒仪器厂提供)。黄铜(H62),金属成分见表1;试剂均为分析纯;溶液用去离子水配制。

表1 铝合金成分Tab.1 Aluminum alloy component %
1.2 静态失重法
静态失重法采用的实验材质是铝合金(6063)标准挂片,规格为50mm×25mm×2mm。使用前,先用丙酮脱脂、蒸馏水冲洗、乙醇2次脱脂后,于室温下晾干。精密称量(±0.1mg),将3片铝合金挂片悬挂于温度为(20±0.1)℃、含有一定浓度缓蚀剂的100mg/L二氧化氯溶液中,恒温放置72h。取出铝合金片,去除表面腐蚀产物,用蒸馏水清洗、乙醇脱脂后置于烘箱中,于50℃烘干1h,称重,停止实验。根据式(1)和式(2)分别计算金属的腐蚀速率R(mm·a-1)及缓蚀率IE。
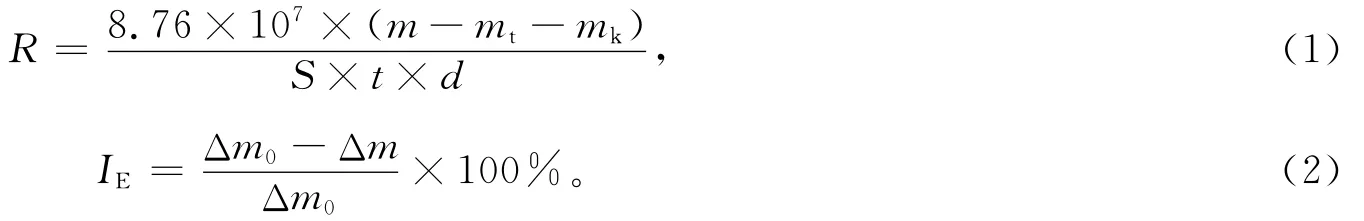
式中:m为实验前金属片质量,g;mt为实验后金属片质量,g;mk为化学处理去除腐蚀产物样片失重值,g;S为金属片的表面积总值,cm2;t为实验时间,h;d为金属材料的密度,kg/m3;Δm0,Δm为不含和含缓蚀剂时的失重量,g。
1.3 动电位极化曲线法
进行动电位极化测量时,以环氧树脂灌封工作电极,保持最终暴露面积为7mm2。实验前,以1200#金相砂纸打磨金属暴露面至光亮无痕;再用无水乙醇擦拭脱脂后,浸泡于100mg/L的二氧化氯溶液中(温度为(20±0.1)℃),极化2h使电位稳定。辅助电极为铂电极,参比电极为饱和甘汞电极(SCE),所有电位均相对于SCE。参数设置如下:扫描速度为0.5mV/s,电位扫描幅度范围为-300~300mV。根据式(3)计算金属的缓蚀率IE。

2 结果与讨论
2.1 硝酸钠对铝合金的缓蚀性能
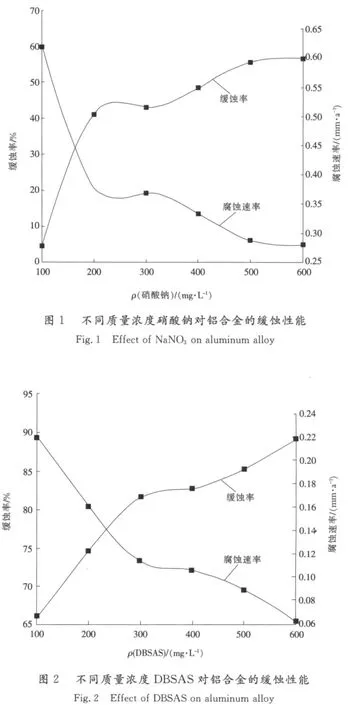
硝酸钠属于钝化膜型缓蚀剂[7],能使金属表面形成一层致密牢固的钝化膜,造成金属的离子化过程受阻。图1为(20±0.1)℃下缓蚀剂质量浓度(ρ)与铝合金片的腐蚀速率(R)及缓蚀率(IE)的关系图。由图1可知:在100mg/L二氧化氯溶液中,硝酸钠对铝合金有一定的缓蚀作用,且随质量浓度的增加,缓蚀率呈递增趋势;当缓蚀剂质量浓度为500mg/L时,其对铝合金的缓蚀率为55.58%,此后缓蚀率随浓度的变化趋于平缓。分析其原因可能如下[8-10]:可能会与二氧化氯水溶液中存在的微量和在金属表面发生竞争性吸附,并在铝表面形成致密钝化膜,其主要成分是γ-Al2O3。随着硝酸钠质量浓度的增大,金属钝化膜越致密完整,腐蚀微电池存在的可能性越低,可以更为有效地阻碍金属的离子化过程,即阻止金属离子穿过膜向溶液扩散以及腐蚀介质中Cl-向金属表面的迁移。当硝酸钠质量浓度达到一定程度之后,其在铝表面的吸附趋于饱和,从而导致缓蚀率变化趋于平缓。
2.2 DBSAS对铝合金的缓蚀性能
DBSAS是一种阴离子型表面活性剂,可在水溶液中电离出烷基苯磺酸根离子,吸附于金属表面的活性点,阻滞金属的离子化进程,从而实现缓蚀作用[7]。图2为(20±0.1)℃下,DBSAS质量浓度(ρ)与铝合金片的腐蚀速率(R)及缓蚀率(IE)的关系图。从图2可以看出:DBSAS对铝合金的缓蚀率随质量浓度的增大而逐渐提高,当缓蚀剂质量浓度为600mg/L时,其对铝合金的缓蚀率为89.33%。分析其原因可能如下[11-12]:DBSAS在溶液中电离出带负电荷的烷基磺酸根离子,通过静电作用吸附于带正电荷的铝表面,且采取亲水基朝向铝表面、疏水基朝向介质的吸附方式;当缓蚀剂质量浓度增大时,其在铝表面上的吸附覆盖度不断增加,越来越有效地阻碍了腐蚀介质中Cl-与铝表面的接触,使缓蚀率提高。
2.3 硝酸钠和DBSAS的缓蚀协同效应
硝酸钠单独使用时投加量比较大,且缓蚀率不高,但硝酸钠本身所具有的弱氧化性使其可以和有机缓蚀剂之间产生良好的缓蚀协同效应。将硝酸钠与DBSAS进行复配,在100mg/L二氧化氯溶液中,保持缓蚀剂总量不变(300mg/L),改变硝酸钠与DBSAS质量比,进行铝合金的静态失重实验,结果见图3。
由图3可以看出,硝酸钠和DBSAS有显著的协同效应,当硝酸钠和DBSAS的质量比为3∶7时,复配缓蚀剂的缓蚀效果最好,对铝合金的缓蚀率可达96.28%。分析其原因可能如下:铝合金在与二氧化氯的弱酸性介质接触中,金属带正电,对和烷基苯磺酸根离子均具有静电吸附作用,二者在金属表面发生竞争性吸附;同时,二者之间存在相互作用力,从而提高了金属保护膜的覆盖度和稳定性,进一步有效阻止了二氧化氯溶液中微量Cl-与金属基体的接触,避免了金属点蚀的危害,使二者呈现出良好的缓蚀协同效应。
2.4 动电位极化曲线分析
(20±0.1)℃条件下,铝合金在100mg/L的二氧化氯溶液中的极化曲线测定结果见图4,缓蚀剂质量浓度均为300mg/L,硝酸钠、DBSAS以3∶7(质量比)复配。由图4所得电化学数据见表2。

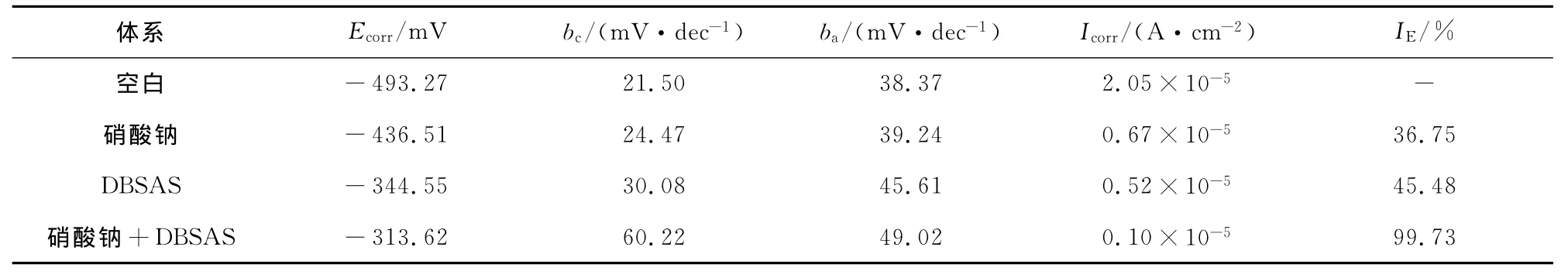
表2 图4所得电化学数据Tab.2 Data from figure 4
综合图4和表2可以看出:在100mg/L二氧化氯溶液中,与空白试验的极化曲线相比,缓蚀剂硝酸钠使铝合金的自腐蚀电位正向移动,自腐蚀电流密度降低,极化曲线的阴、阳两极均受到一定程度的抑制作用。这意味着硝酸钠在二氧化氯介质中属于阳极抑制为主的混合抑制型缓蚀剂。其主要作用机理如下:介于二氧化氯溶液的弱酸性特点,硝酸钠在提高析氢反应过电位的同时,可在金属表面生成薄的氧化膜,将金属和腐蚀介质隔离开来,增大了金属离子转入溶液中的势垒,从而减缓金属的腐蚀。缓蚀剂DBSAS使铝合金的自腐蚀电位发生显著的正向位移,自腐蚀电流密度降低,阳极和阴极极化曲线的塔菲尔斜率均增大。可以推断,DBSAS在二氧化氯溶液中属于阳极抑制为主的混合抑制型缓蚀剂,即DBSAS在二氧化氯溶液中不仅与Cl-在铝合金表面发生竞争性吸附,抑制阳极金属的离子化进程,同时对阴极去极化进程起到了一定的抑制作用。将硝酸钠和DBSAS以3∶7(质量比)复配之后,铝合金的自腐蚀电位显著正移,自腐蚀电流密度明显降低,阳极和阴极极化曲线的塔菲尔斜率增大。可以认为:将具有不同电化学作用机理的2种缓蚀剂配合使用,可以得到良好的缓蚀协同效应。该结果与静态失重实验的结果一致。
2.5 电镜扫描显微镜(SEM)分析
将铝合金浸泡于100mg/L二氧化氯溶液中进行电镜验证,图5是铝合金浸泡24h之后放大800倍的效果图。图5a)是未进行浸泡的铝合金新片,表面平整,可见打磨痕迹;将铝合金直接浸泡于未加缓蚀剂的100 mg/L二氧化氯溶液中,形貌图见图5b),铝合金表面发生了严重的腐蚀,且存在明显的点蚀现象,其原因可能是二氧化氯中存在的Cl-所致;图5c)是将铝合金浸泡于加有300mg/L缓蚀剂(即硝酸钠与DBSAS以质量比为3∶7进行复配)的二氧化氯溶液中的形貌图,可以看出,铝合金表面已生成一层较为致密的保护膜,存在轻度的龟裂现象。SEM验证结果与以上实验结果一致,即硝酸钠与DBSAS以质量比为3∶7进行复配对铝合金产生了良好的防腐蚀效果。

图5 铝合金的SEM形貌图Fig.5 SEM of aluminum alloy sheet
3 结 语
1)在100mg/L二氧化氯介质中,单独添加硝酸钠,其对铝合金的缓蚀率随缓蚀剂质量浓度的增大而增大,当质量浓度为500mg/L时,缓蚀率为55.58%,之后缓蚀率随质量浓度变化趋于平缓;单独添加DBSAS,其缓蚀率随缓蚀剂质量浓度的增大而提高,当质量浓度为600mg/L时,对铝合金的缓蚀率可达89.33%。
2)当硝酸钠与DBSAS复配总质量浓度为300mg/L时,若二者质量比为3∶7,则可对铝合金产生显著的缓蚀协同效应,缓蚀率达到96.28%,明显降低了硝酸钠和DBSAS的用量,即在实现良好缓蚀效果的同时降低了缓蚀剂的总质量浓度。
[1] 张文清,蒋 励,何友兰.二氧化氯的性质及用于水消毒的优点[J].中国消毒学杂志(Chinese Journal of Disinfection),2000,17(4):220-221.
[2] 曹楚南.腐蚀电化学原理[M].北京:化学工业出版社,2008.
[3] 王奎涛,张炳烛,李彦红,等.高效、高纯稳定二氧化氯溶液生产技术关键因素的优化[J].河北科技大学学报(Journal of Hebei University of Science and Technology),2004,25(3):88-90.
[4] 王奎涛,陈宏槟,冀维锋,等.速溶型二氧化氯泡腾片的杀菌效果试验及现场应用[J].河北科技大学学报(Journal of Hebei University of Science and Technology),2009,30(1):45-50.
[5] 康志娟,王奎涛,赵海栋,等.常见金属在二氧化氯消毒液中的腐蚀情况[J].腐蚀与防护(Corrosion and Protection),2010,31(12):984-985.
[6] 黄君礼.水消毒剂和处理剂——二氧化氯[M].北京:化学工业出版社,2010.
[7] 张天胜,张 浩,高 红,等.缓蚀剂[M].北京:化学工业出版社,2008.
[8] 周 俊,王七芬,刘晓轩,等.硝酸根离子对铝在盐酸溶液中的缓蚀作用[J].清洗世界(Cleaning World),2006,22(6):1-4.
[9] BETHENCOURT M,BOTANA F J,CALVINO J J,et al.Lanthanide compounds as environmentally-friendly corrosion inhibitors of aluminium alloys:A review[J].Corrosion Science,1998,40(11):1 803-1 819.
[10] QU Qing,LI Lei,BAI Wei,et al.Sodium tungstate as a corrosion inhibitor of cold rolled steel in peracetic acid solution original research article[J].Corrosion Science,2009,51(10):2 423-2 428.
[11] ZHAO Tian-pei,MU Guan-nan.The adsorption and corrosion inhibition of anionic surfactants on aluminium surface in hydrochloric acid[J].Corrrosion Science,1999,41(10):1 937-1 944.
[12] 谷 宁.表面活性剂与缓蚀剂协同效应的研究[J].河北省科学院学报(Journal of the Hebei Academy of Sciences),2001,18(4):231-233.
Synergistic corrosion inhibition effect of sodium nitrate and DBSAS on aluminum alloy in chlorine dioxide solution
WANG Kui-tao1,2,LU Nan1,2,GAO Jin-long1,2,WU Hai-xia1,2,LI Wen-ya1,2
(1.College of Chemical and Pharmaceutical Engineering,Hebei University of Science and Technology,Shijiazhuang Hebei 050018,China 2.Hebei Research Center of Pharmaceutical and Chemical Engineering,Hebei University of Science and Technology,Shijiazhuang Hebei 050018,China)
Synergistic inhibition effect of sodium nitrate and dodecylbenzenesulfonic acid sodium(DBSAS)on aluminum alloy in 100mg/L chlorine dioxide solution was studied by method of weight loss,polarization curves and SEM.The results show that NaNO3has little inhibition effect on aluminum alloy corrosion,and the corrosion inhibition efficiency is only 55.58%.DBSAS has better inhibition effect on aluminum alloy corrosion,and the corrosion inhibition efficiency is up to 89.33%.The complex of NaNO3and DBSAS has good synergistic inhibition effects.When the mass ratio of NaNO3to DBSAS is 3∶7,the complex shows best inhibition effect on aluminum alloy corrosion,and the corrosion inhibition efficiency reaches 96.28%.
chlorine dioxide;aluminum alloy;sodium nitrate;DBSAS;inhibitor;synergistic effect
O635
A
1008-1542(2012)03-0215-05
2011-12-16;
2012-03-09;责任编辑:张士莹
王奎涛(1962-),男(回族),河北石家庄人,教授,硕士,主要从事二氧化氯工艺开发方面的研究。
