盐酸体系中电沉积制备砷锑合金
2012-12-14曹华珍万强波单海鹏阮慧敏郑国渠
曹华珍,万强波,单海鹏,阮慧敏,郑国渠
(浙江工业大学 化学工程与材料学院,杭州 310014)
砷锑合金在电子、光电领域的应用是近年来的研究热点[1]。光电探测器、光学气体传感器等光电设备中均用到砷锑合金。砷是砷锑合金的主要成分,从含砷废水中电沉积制备单质砷不仅可以缓解砷污染问题,而且可以获得有应用价值的单质砷,因此曾引起众多学者的研究兴趣[2-7]。然而,有关单质砷的电沉积存在诸多问题,亟待进一步的解决,其中最重要的是阴极过程产生的大量剧毒的 AsH3气体[8],AsH3的生成消耗了阴极还原的单质砷,从而随电沉积时间的延长,砷沉积的电流效率急剧下降。至今仍无有效措施抑制 AsH3气体的产生,因此,有关砷的电沉积有待进一步深入研究。
近年来,有关电沉积砷合金的研究报道越来越多[9-11]。由于共沉积金属的存在,一定程度上改善了沉积层的导电性,同时也可有效抑制 AsH3气体的析出。CATTARIN 等[12]以 Ni、Ti为基体,在酒石酸溶液中电沉积制备了 InAsxSb1-x合金,合金表面均匀、平整。BERTONCELLO等[13]从SbCl3和NaAsO2的柠檬酸溶液中采用阴极电沉积获得了砷含量为23% (质量分数)和42%的砷锑合金。MARCO等[14]提出柠檬酸用于砷锑合金的电沉积,可以有效地抑制析氢反应,提高电流效率,改善沉积层质量。然而在盐酸体系中有关砷锑合金的电沉积研究未见文献报道。
本研究小组在前期进行氯化浸出处理含砷锑的铅阳极泥过程中,产生大量的含砷盐酸水溶液[15],在此,本文作者采用电沉积方法从含砷锑的盐酸水溶液中制备砷锑合金。利用循环伏安、计时电流暂态技术研究了盐酸体系中砷锑合金的阴极电结晶过程,结合SEM和EDS分析,确立了盐酸体系中电沉积砷锑合金的有利条件,为高酸性条件下砷锑合金的电沉积提供一定的依据。
1 实验
含砷锑的铅阳极泥经过氯化浸出得到砷锑盐酸水溶液,经过二次蒸馏分离后得到纯净的 AsCl3盐酸水溶液和SbCl3盐酸水溶液,即可配制不同浓度As3+、Sb3+、HCl以及柠檬酸的电解液。在所配制的电解液中,以石墨作为阳极,铜作为阴极采用恒电流(1 mA/cm2)方式进行电沉积制备砷锑合金,沉积时间为2 h。阴极析出的AsH3气体通过N2排出到500 mL 0.1 mol/L的NaClO溶液中氧化吸收,利用电感耦合等离子体质谱仪分析吸收液中As含量。采用 Hitachi S-4700扫描电镜观察沉积物的表面微观形貌,采用X射线能谱仪(EDS)分析沉积物的化学元素组成。
采用 CHI660电化学工作站测试循环伏安曲线、电流—时间暂态曲线。循环伏安曲线的测试装置采用传统的三电极电解槽,对电极为铂电极,饱和甘汞电极作为参比电极。工作电极采用铜电极,裸露面积为1 cm2,其余部分用环氧树脂密封,扫描电位范围为-400~80 mV,扫描速率为100 mV/s。采用玻碳电极(工作面积为0.125 6 cm2)测试电流—时间暂态曲线,研究砷锑在玻碳电极上的电化学形核。每次测定之前,工作电极均在氧化铝抛光介质作用下于金丝绒布上抛光至镜面,并采用无水乙醇除油。
2 结果与讨论
2.1 循环伏安研究
2.1.2 盐酸浓度的影响
图1所示为在As3+浓度0.04 mol/L、Sb3+浓度0.01 mol/L、不同盐酸浓度的电解液中得到的循环伏安曲线。从图1可以观察到,电位在-0.20~-0.35 V之间存在着明显的阴极电流峰,说明在此电位下有电子得失反应发生,对应于砷锑的还原。盐酸浓度为 2、3、4 mol/L时所对应的峰电位分别为-0.24、-0.28和-0.33 V,即随着盐酸浓度增大,阴极峰电位负移,说明H+的加入增大了砷锑还原的过电位。
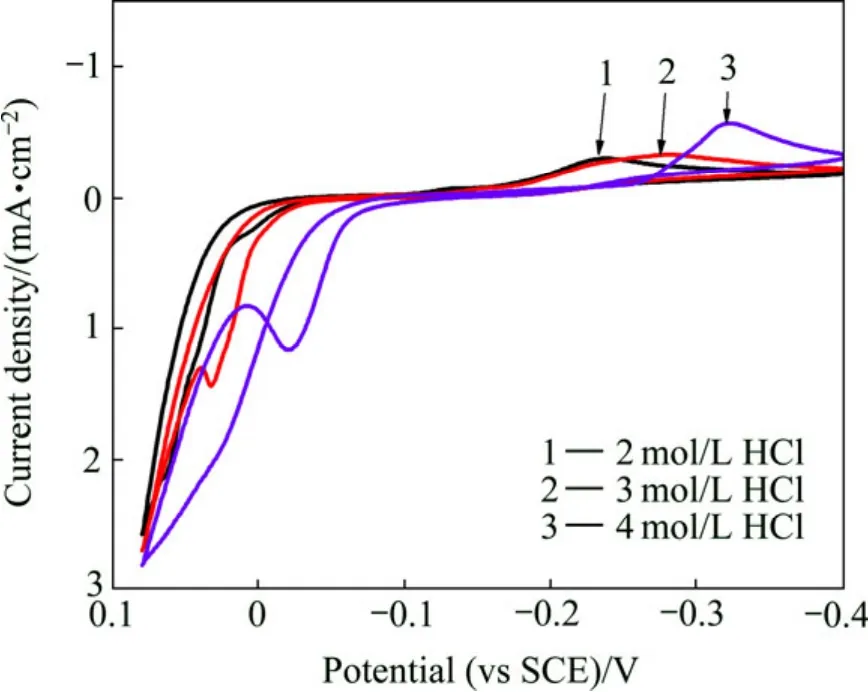
图1 盐酸浓度对循环伏安曲线的影响Fig.1 Effect of hydrochloric acid concentrations on cyclic voltammograms at As3+ concentration of 0.04 mol/L and Sb3+concentration of 0.01 mol/L
2.1.2 Sb3+浓度的影响
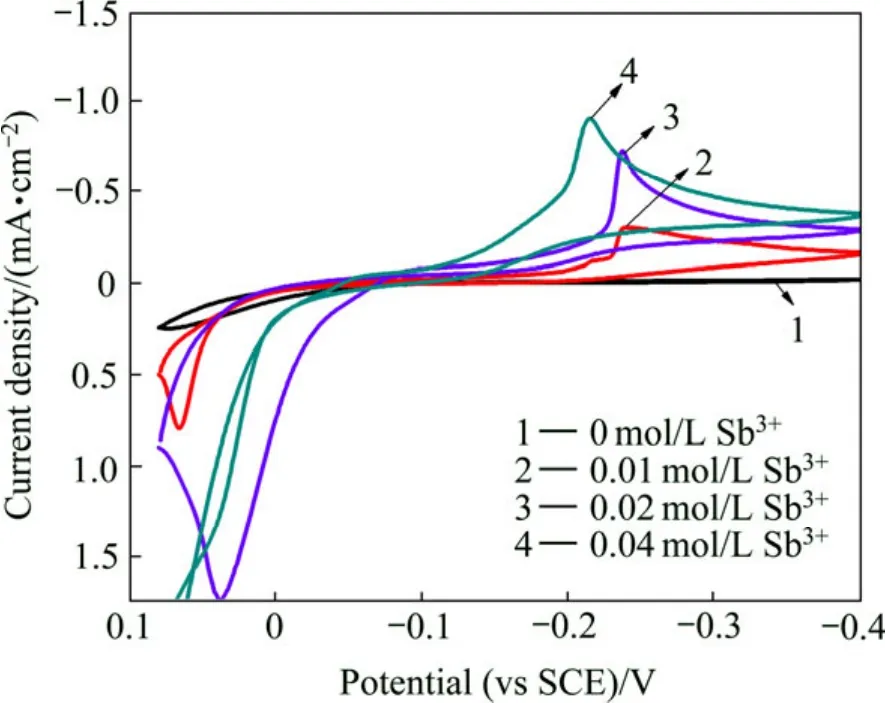
图2 Sb3+浓度对循环伏安曲线的影响Fig.2 Effect of Sb3+ concentrations on cyclic voltammograms at As3+ concentration of 0.04 mol/L and HCl concentration of 2 mol/L
图2所示为在盐酸浓度 2 mol/L、As3+浓度 0.04 mol/L时不同 Sb3+浓度的电解液中得到的循环伏安曲线。从图2可以看到,不含Sb3+时,在扫描电位范围内没有出现明显的阴极电流峰,说明在此条件下As3+的还原困难。Sb3+加入到砷电解液中,循环伏安曲线上出现了明显的阴极还原峰。随着 Sb3+的浓度从 0.1 mol/L增加至0.4 mol/L,阴极峰电位也从-0.24 V逐渐正移至-0.21 V,表明加入Sb3+使金属还原的过电位减小,有利于合金沉积。
2.1.3 柠檬酸的影响
图3所示为在盐酸浓度 2 mol/L、As3+浓度 0.04 mol/L、Sb3+浓度0.01 mol/L的条件下加入柠檬酸后的循环伏安曲线。从图3可以看到,随着柠檬酸的加入,金属还原的峰电位逐渐负移,即沉积过电位增大,这是由于柠檬酸在溶液中与金属离子发生了络合,从而导致还原电位发生改变。
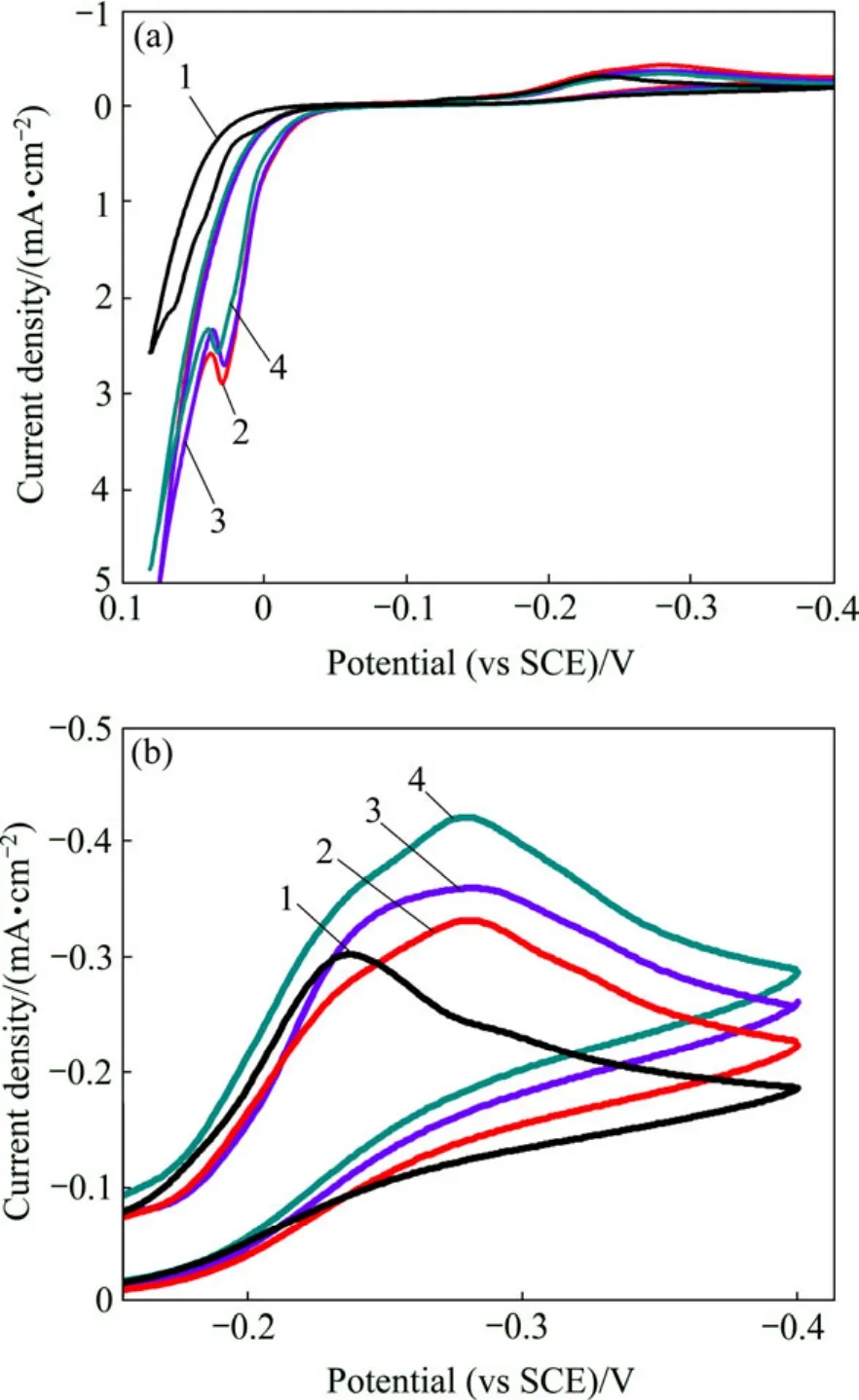
图3 柠檬酸浓度对循环伏安曲线的影响Fig.3 Effect of citric acid on cyclic voltammograms at As3+concentration of 0.04 mol/L, Sb3+ concentration of 0.01 mol/L and HCl concentration of 2 mol/L: 1—0 mol/L citric acid; 2—0.2 mol/L citric acid; 3—0.4 mol/L citric acid; 4—0.6 mol/L citric acid;
2.2 电结晶过程
2.2.1 在玻碳电极上的电结晶初期行为
图4所示为玻碳电极在含砷锑的盐酸电解液中的循环伏安曲线。从图4可以看到,电位正向回扫时通过的阴极电流大于负向扫描时的阴极电流,出现了明显的电流环,这是形核与生长过程的典型特征。
图5所示为玻碳电极在含砷锑的盐酸电解液中不同阶跃电位下的电流—时间暂态曲线。曲线的典型特征为在电位阶跃初期极短时间内,暂态电流迅速上升达到最大值,之后暂态电流衰减并逐渐趋于稳定。此时,电结晶过程经历了生长中心的交叠并向外生长伸向溶液,同时伴随生长中心的消失和新生长中心的再生。随阶跃电位的负移,即过电位增大,峰电流(Ⅰm)增大,其对应的时间tm呈规律性的缩短,说明过电位升高导致成核速率加快,成核诱导时间缩短。
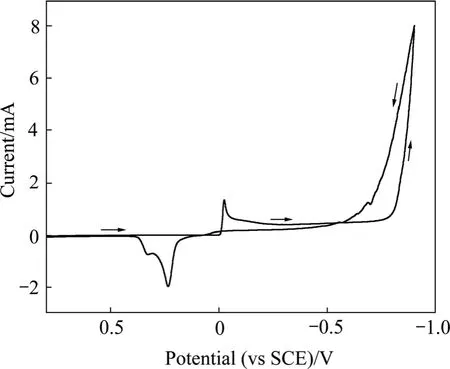
图4 玻璃碳电极在砷锑盐酸电解液中的循环伏安曲线Fig.4 Cyclic voltammogram of glassy carbon in electrolyte containing As3+ and Sb3+ and hydrochloric acid (As3+concentration of 0.04 mol/L; Sb3+ concentration of 0.01 mol/L;HCl concentration of 2 mol/L)
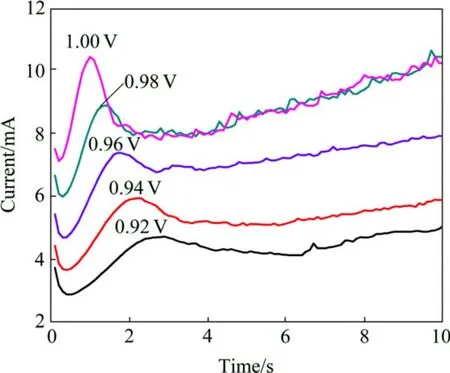
图5 不同阶跃电位下的电流—时间暂态曲线Fig.5 Current—transient time curves at different applied potentials (As3+ concentration: 0.04 mol/L; Sb3+ concentration of 0.01 mol/L; HCl concentration of 2 mol/L)
SHARIFKER等[16]曾导出液相传质控制时半球晶核三维生长的电流表达式:
瞬时成核,
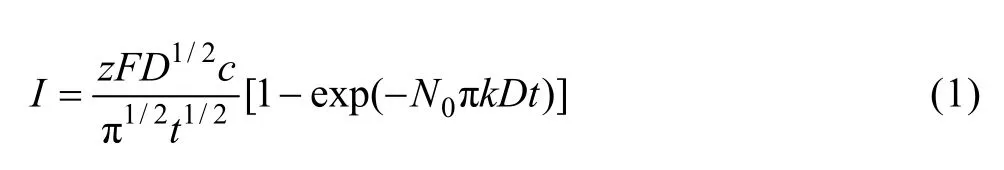
连续成核,
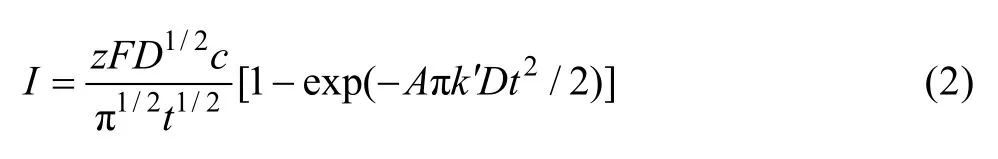
式中:zF为沉积离子的摩尔电荷;D为沉积离子的扩散系数;c为沉积离子的浓度;k和k’为常量;N0为晶核密度;A为成核速度常数。
通过微分变换,利用各暂态的最大值(Ⅰm,tm),可得到相应的无量纲形式:
瞬时成核,
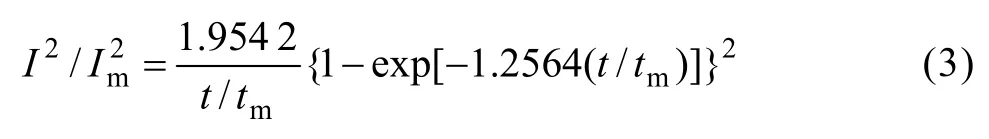
连续成核,
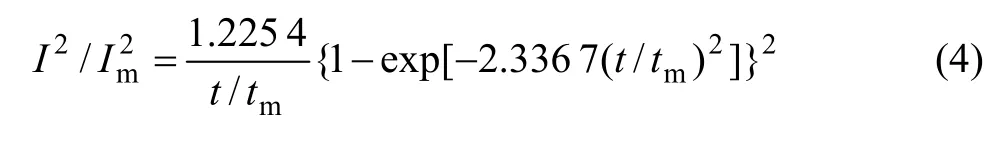
瞬时成核与连续成核是描述成核速度常数很大和很小的两种极端情况。由图5得到的无因次曲线Ⅰ2/Ⅰm2—t/tm以及瞬时成核、连续成核的理论曲线均绘于图6中。从图6可以看到,瞬时成核呈现一较宽的峰,而连续成核曲线的峰相对尖锐。实验所测数据均与连续成核曲线接近,说明此条件下的形核速率非常小。
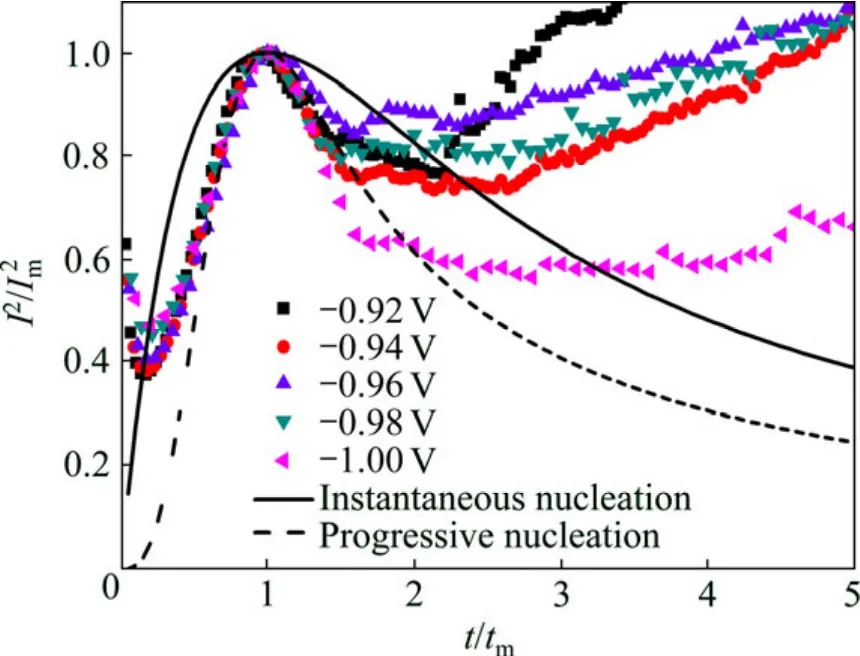
图6 在砷锑盐酸电解液中的 Ⅰ2 /Ⅰm2—t/tm无因次曲线图Fig.6 Non-dimensional plots of Ⅰ2/Ⅰm2 —t/tm in solution containing As3+, Sb3+ and hydrochloric acid (As3+ concentration of 0.04 mol/L; Sb3+ concentration of 0.01 mol/L; HCl concentration of 2 mol/L)
2.2.2 柠檬酸的影响
图7所示为砷锑盐酸电解液中加入了柠檬酸后的Ⅰ2/Ⅰ2—t/tm无因次曲线图。从图7可以看出,各阶跃m电位下的无因次曲线均介于瞬时成核与连续成核理论曲线之间。与图5未加柠檬酸的无因次曲线相比,加入柠檬酸后无因次曲线的峰变宽,说明形核速率增大。这是由于柠檬酸的络合作用增大了合金在玻碳电极上的结晶过电位,促进了晶核的形成,从而也有利于获得细小晶粒,提高沉积层的质量。
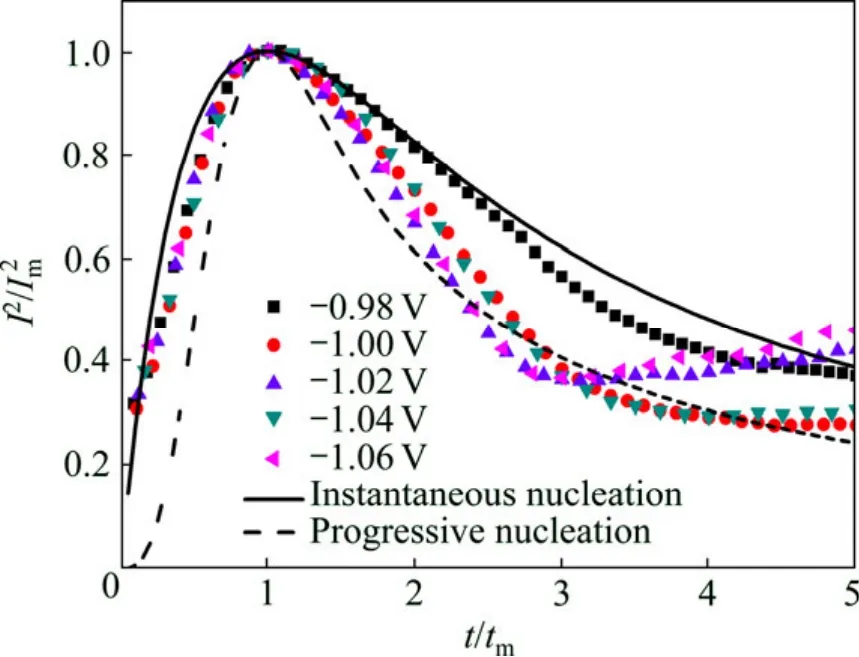
图7 加入柠檬酸后的 Ⅰ2/Ⅰm2—t/tm无因次曲线Fig.7 Non-dimensional plots of Ⅰ2 /Ⅰm2—t/tm in system containing citric acid (As3+ concentration of 0.04 mol/L; Sb3+concentration of 0.01 mol/L; HCl concentration of 2 mol/L;citric acid concentration of 0.4 mol/L)
2.2.3 锑离子浓度的影响
图8所示为锑离子浓度较高条件下的Ⅰ2/Ⅰm2—t/tm无因次曲线。从图8可以看到,各阶跃电位下的无因次曲线均与瞬时成核曲线接近,说明此条件下的形核速率非常大。与图7中锑离子浓度较低条件下的无因次曲线相比,发现随着锑离子浓度增大,无因次曲线的峰变宽,有利于金属在玻碳电极上的形核。这是由于砷锑合金中,砷导电性差、活性低,形核过程易发生在导电性较好的锑表面,当电解液中锑浓度增大,电沉积层中的锑含量也会相应增加,因而形核活性点数目增多,形核速率增大。
2.2.4 盐酸浓度的影响
图9所示为较高酸度(4 mol/L HCl)条件下的Ⅰ2/Ⅰm2—t/tm无因次曲线。与图7较低酸度(2 mol/L HCl)条件下的无因次曲线相比,可以看出酸度增加使无因次曲线的峰变得更宽,形核速率增大,可以获得更细小晶粒。这是由于在电沉积的过程中,惰性阳离子H+的加入有利于合金析出过电位的提高,从而促进了形核过程。
2.3 阴极产物分析
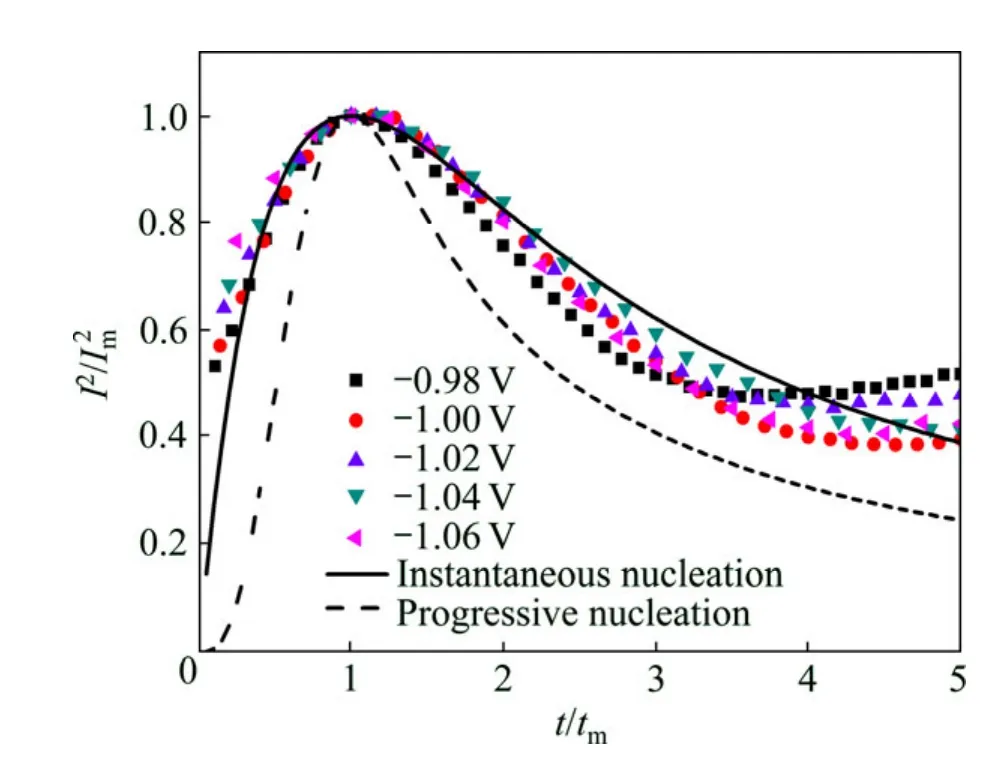
图8 锑离子浓度较高条件下的 Ⅰ2 /Ⅰm2—t/tm无因次曲线Fig.8 Non-dimensional plots of Ⅰ2/Ⅰm2 —t/tm in system with high concentration of Sb3+ (As3+ concentration of 0.04 mol/L;Sb3+ concentration of 0.01 mol/L; HCl concentration of 2 mol/L; citric acid concentration of 0.4 mol/L)
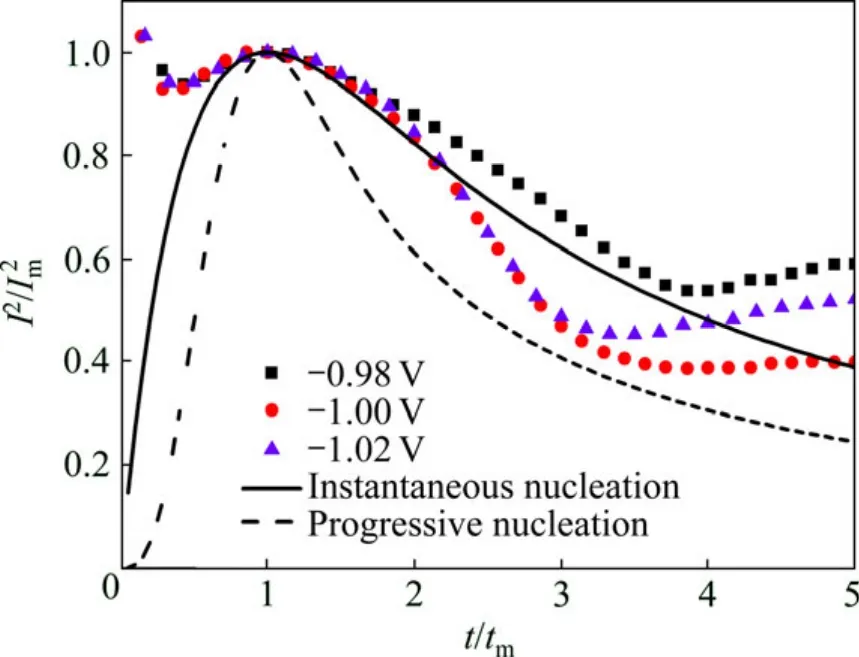
图9 较高酸度条件下的 Ⅰ2/Ⅰm2—t/tm曲线Fig.9 Non-dimensional plots of I Ⅰ2/Ⅰm2 —t/tm in system with high concentration of hydrochloric acid (As3+concentration of 0.04 mol/L; Sb3+ concentration of 0.01 mol/L;HCl concentration of 2 mol/L; citric acid concentration of 0.4 mol/L)

图10 不同条件下电沉积制备的砷锑合金的表面形貌Fig.10 Surface morphologies of AsSb alloy electrodeposited under different conditions: (a) 0.04 mol/L As3+, 0.01 mol/L Sb3+,2 mol/L H+; (b) 0.04 mol/L As3+, 0.01 mol/L Sb3+, 2 mol/L H+, 0.04 mol/L citric acid; (c) 0.04 mol/L As3+, 0.02 mol/L Sb3+, 2 mol/L H+; (d) 0.04 mol/L As3+, 0.01 mol/L Sb3+, 4 mol/L H+
图10所示为不同条件下制备的砷锑合金表面微观形貌。在As3+0.04 mol/L、Sb3+0.01 mol/L、H+2 mol/L的电解液中制备的沉积层晶粒粗大,表面粗糙;加入柠檬酸或锑离子溶度增加,均使沉积层的晶粒尺寸减小,尤其是柠檬酸的加入明显改善了表面平整度;高酸度条件下,沉积物的晶粒更加细小,但由于产生了粉末状沉积物,无法获得致密的合金沉积层。EDS谱与计时电流暂态分析结果相吻合,都证实了电沉积砷锑的有利条件是在砷电解液中加入一定浓度的Sb3+离子和柠檬酸,同时控制适当的酸度,可以获得高质量的砷锑合金。图11所示为沉积物的EDS谱,证实了阴极沉积物含有砷、锑。图谱中的铜是电极基体,Pt的存在是由于试样表面进行了喷金处理,少量的 Cl-是电解过程中由于夹杂作用进入沉积层中。表1列出不同组成的电解液中得到的沉积物的砷锑比。由表1可以看出,电解液的组成是决定沉积层中砷、锑比的关键。在As3+0.04 mol/L,Sb3+0.01 mol/L,H+2 mol/L的电解液中制备的合金其砷锑摩尔比为1:1,电解液中锑离子浓度的增加或加入柠檬酸络合剂,都将使沉积层中的锑含量大大增加,而电解液中酸度的改变,对沉积层中的砷锑比影响不大。
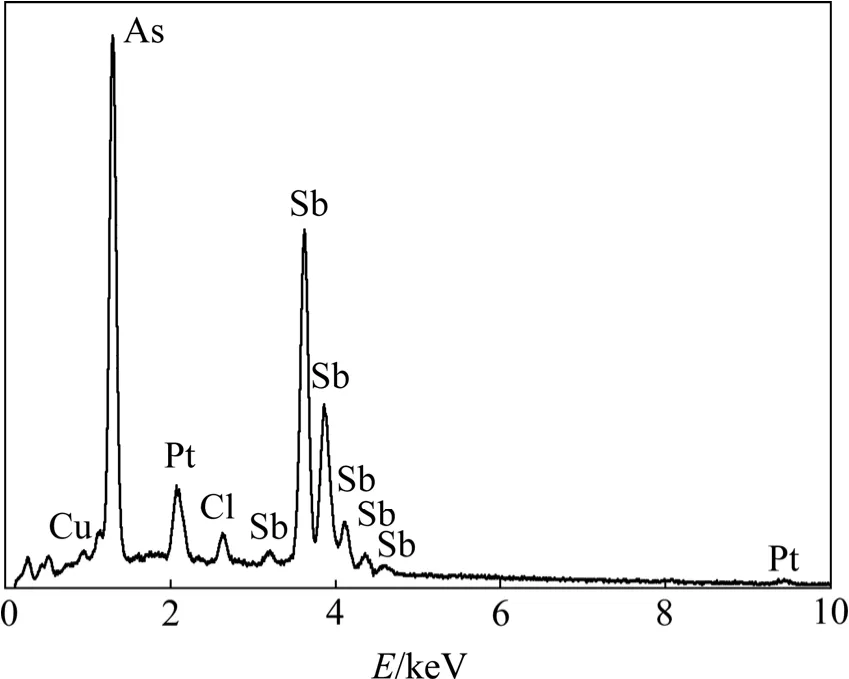
图11 阴极沉积物的EDS谱Fig.11 EDS spectrum of deposits in cathode
表2所列为不同沉积条件下AsH3气体的析出量。在含砷溶液中电解,其阴极过程不仅有金属沉积物析出,同时不可避免产生AsH3气体。有关AsH3气体的析出,BRUSCIOTTI等[7]进行了系统的研究,发现随电流密度的增加,AsH3气体的析出量逐渐增大。从表2可以看到,在只含砷的电解液中,电极材料影响AsH3气体的析出,采用铜电极且在非常小的电流密度条件下,其AsH3气体的析出量占总电量的7.8 %;而在含砷锑的盐酸水溶液中,采用了较高的电流密度,AsH3气体量只占总电量的 2.12%。这说明本研究所采用的电解液体系可以有效地抑制 AsH3气体的析出。这主要是由于 AsH3气体的析出反应是在电沉积砷的表面进行,由于共沉积金属锑的存在,减少了 AsH3气体析出的活性点,从而抵制了AsH3气体的产生。
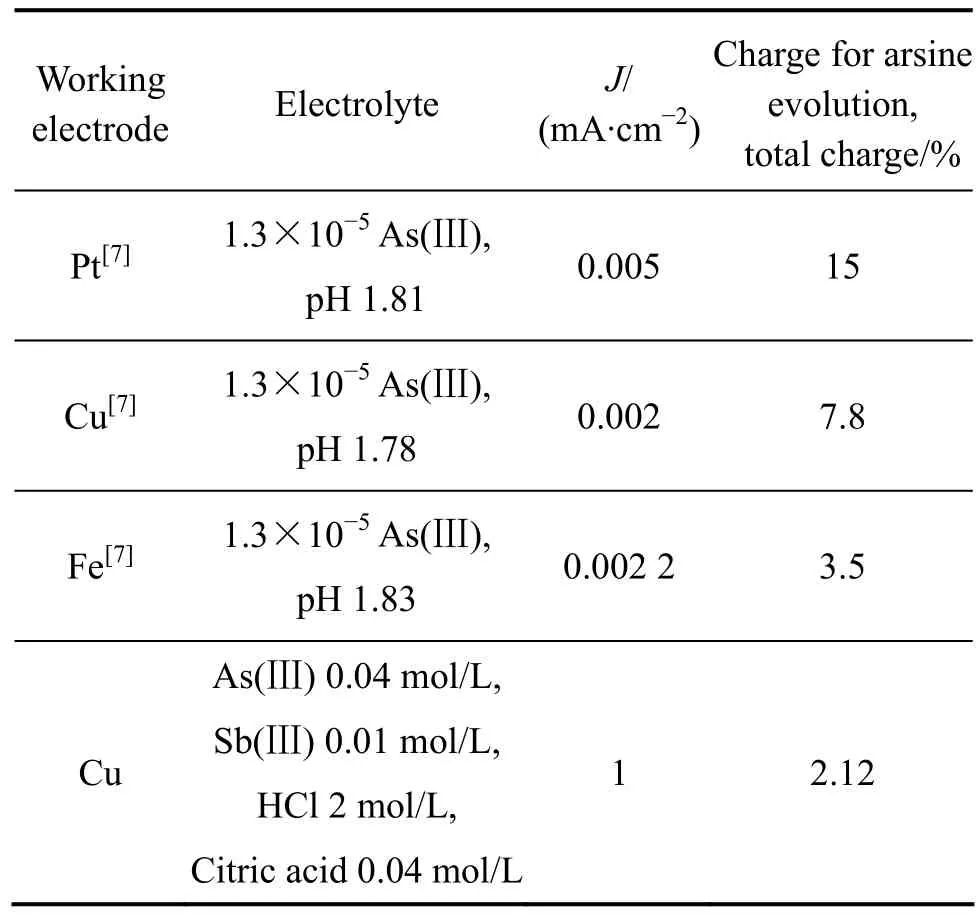
表2 不同沉积条件下AsH3气体的析出量Table2 Evolution of arsine at different conditions
3 结论
1)在含砷锑的盐酸水溶液中通过恒电流沉积可以制备砷锑合金,且有效抑制了AsH3气体的析出。
2) 砷锑合金在玻碳电极上的电结晶遵循液相传质控制的三维生长机理,形核速率受到电解液中各组分的影响。随着Sb3+浓度、HCl浓度增加以及柠檬酸络合剂的加入,其形核速率增大。
3) 加入柠檬酸或锑离子浓度增大均使沉积物的晶粒尺寸减小,提高沉积层的表面平整度;酸度增加可进一步细化晶粒,但酸度过高将产生粉末状沉积物。
4) 电解液的组成影响沉积层中的砷锑比,锑离子浓度的增大或柠檬酸络合剂加入,都将使沉积层中砷的比例大幅减小;而电解液酸度的改变,对沉积层中的砷锑比影响不大。
5) 电沉积的最佳工艺如下:0.04 mol/L As3+、0.01 mol/L Sb3+、2 mol/L HCl、0.04 mol/L柠檬酸,在此条件下可以电沉积获得致密的砷锑合金,同时使沉积层中有较高的砷含量。
[1]BELABBES A, ZAOUI A, FERHAT M.Alloying effect in the III-As-Sb ternary systems[J].Materials Science and Engineering B, 2007, 137: 210-212.
[2]彭想军, 田琦峰, 袁 华, 杜治平, 吴元欣.工业磷酸中As(Ⅲ)的电化学沉积[J].应用化工, 2008, 37(10): 1121-1124.PENG Xiang-jun, TIAN Qi-feng, YUAN Hua, DU Zhi-ping,WU Yuan-xin.Electrodepositon of As(Ⅲ) in technical grade phosphoric acid[J].Applied Chemical Industry, 2008, 37(10):1121-1124.
[3]DINAN T E, JOU W F, CHEH H Y.Arsenic deposition onto a gold substrate[J].J Electrochem, 1989, 136: 3284-3287.
[4]JIA Zheng, SIMM A O, DAI Xuan, COMPTON R G.The electrochemical reaction mechanism of arsenic deposition on an Au(111) electrode[J].Journal of Electroanalytical Chemistry,2006, 587: 247-253.
[5]WEI Z, SOMASUNDARAN P.Cyclic voltammetric study of arsenic reduction and oxidation in hydrochloric acid using a Pt RDE[J].Journal of Applied Electrochemistry, 2004, 34:241-244.
[6]BEJAN D, BUNCE N J.Electrochemical reduction of As(Ⅲ)and As(Ⅴ) in acidic and basic solutions[J].Journal of Applied Electrochemistry, 2003, 33: 483-489.
[7]BRUSCIOTTI F, DUBY P.Co-deposition of arsenic and arsine on Pt, Cu, and Fe electrodes[J].Electrochemistry Communications, 2008, 10: 572-576.
[8]仇勇海, 唐仁衡, 陈白珍.砷化氢析出电势的探讨[J].中国有色金属学报, 2000, 10(1): 101-104.QIU Yong-hai, TANG Ren-heng, CHEN Bai-zhen.Evolution potential of arsine[J].The Chinese Journal of Nonferrous Metals,2000, 10(1): 101-104.
[9]NAYAK J, SAHU S N.Effect of synthesis temperature on the structure and optical properties of electro-chemically grown GaAs nanocrystals[J].Physica E, 2008, 41: 92-95.
[10]NAYAK J, SAHU S N.Orthorhombic-phase GaAs nanoparticles prepared by an electrochemical technique[J].Applied Surface Science, 2004, 229: 97-104.
[11]韩爱珍, 林逸青, 赵永春, 高元恺.GaAs薄膜电沉积的机理与工艺研究[J].大阳能学报, 1997, 18(4): 376-379.HAN Ai-zhen, LIN Yi-qing, ZHAO Yong-chun, GAO Yuan-kai.A study on the mechanism and technology of the GaAs film electrodeposition[J].Acta Energiae Solaris Sinica, 1997 18(4):376-379.
[12]CATTARIN S, MUSIANI M M, CASELLATO U, GUERRIERO P, BERTONCELLO R.Cathodic deposition of ternary In+As+Sb alloys and formation of InAsxSbl-x[J].Journal of Electroanalytical Chemistry, 1995, 308: 209-218.
[13]BERTONCELLO R, GLISENTI A, GRANOZZI G, MUSIANI M M.Angle-resolved X-ray photoelectron spectroscopy contribution to elucidation of the mechanism of cathodic deposition of As-Sb alloys[J].Journal of Electroanalytical Chemistry, 1994, 374: 37-43.
[14]MUSIANI M M, PAOLUCCI F.Electrodeposition of As-Sb alloys[J].Elcctrochimica Acta, 1966, (11): 251-265.
[15]CAO Hua-zhen, CHEN Jin-zhong, YUAN Hai-jun, ZHENG Guo-qu.Preparation of pure SbCl3from lead anode slime bearing high antimony and low silver[J].Transactions of Nonferrous Metals Society of China, 2010, 20: 2379-2403.
[16]SCHARIFKER B, HILLS G.Theoretical and experimental studies of multiple nucleation[J].Electrochim Acta, 1983, 28(7):879-889.
