生物质提取木糖工艺及木糖检测方法研究进展
2012-11-15付文,王丽,史博
付 文,王 丽,史 博
(广东石油化工学院,化工与环境工程学院,广东茂名525000)
生物质提取木糖工艺及木糖检测方法研究进展
付 文,王 丽*,史 博
(广东石油化工学院,化工与环境工程学院,广东茂名525000)
木糖作为一种重要的化工原料,在食品、饮料等行业中应用广泛。综述了生物质制备木糖的工艺进展,对木糖检测方法进行了简单阐述。
木糖,工艺,综述
木糖作为一种重要的化工原料,在食品、饮料等行业中作为理想的甜味剂、营养剂和治疗剂已为国际所公认。除此之外,木糖的相关产品也有很高的功能价值。如木糖(Xylose)经催化加氢可制得木糖醇(Xylitol),木糖醇甜度和发热量同蔗糖相当,但糖尿病人也可食用;还具有防龋功能,发达国家已广泛用作食品添加剂;它还是国防、塑料、医药等工业的重要原料,有广阔的市场和发展前景。因此,木糖的生产与分析工艺对木糖及木糖相关行业的发展十分重要。综述了生物质制备木糖的工艺进展,对木糖检测方法进行了简单阐述。
1 木糖的性质与功能
D-木糖(D-xylose)是戊糖的一种,分子量为150.14,和阿拉伯糖、核糖同属于五碳糖,化学结构式见图1。其性状为白色针状结晶或结晶性粉末,无毒、无臭,具有清凉甜味,易溶于水,难溶于乙醇,有右旋光性和变旋光性。木糖是木聚糖的一个组分,广泛存在于植物中,也存在于动物肝素、软骨素和糖蛋白中,是某些糖蛋白中糖链与丝氨酸(或苏氨酸)的连接单位[1]。
木糖作为一种功能性食品的基料,具有以下主要功能:促进益生菌-双歧杆菌的增殖,减少有毒发酵产物及有害细菌酶的产生,改善人体的微生物环境,提高机体的免疫能力;抑制病原菌的产生,防止腹泻;抑制口腔病菌的滋生,防止龋齿;具备膳食纤维的部分生理功能,有降血压血脂,降胆固醇及预防肠癌的作用;食物的配伍性好。木糖与钙同时摄入,可以提高人体对钙的吸收率和保留率。

图1 D-木糖的结构式Fig.1 The structural formular of D-xylose
2 木糖制备原料来源
在自然界,木糖多以缩聚状态广泛存在于自然界植物的半纤维素中,即以大分子的多缩戊糖(木聚糖)的形式存在于植物体内。大量的科学研究结果证明,半纤维素几乎存在于所有的植物细胞壁当中,是植物细胞壁的三大组织之一。统计资料表明,全球的植物每年生成的半纤维素有3.5×1010t之多,半纤维素是地球上最丰富、最廉价的可再生资源之一。从理论角度讲,只要含有半纤维素的植物均可作为木糖的生产原料,植物细胞壁中的纤维素和木质素是由聚糖混合物紧密地相互贯穿在一起的,此聚糖混合物被称为半纤维素[2],因此生产木糖的原料来源比较广泛。一般来说,农业植物纤维废料如玉米芯、棉籽壳、甘蔗渣、稻壳以及其他种子皮壳、一些木科植物等都是制取木糖的理想原料。这些植物废料中含有大约16%~40%的多缩戊糖,而多缩戊糖经水解则可得到高附加值的低聚木糖和木糖。从农作物废料中提取木糖不仅有利于资源的综合利用,而且拓展了制备木糖的原料范围,具有广泛的经济效益与明显的社会效益。表1列举了几种常见的制备木糖的原料及成分。

表1 几种原料的主要成分[3-4]Table 1 The basis of several raw material
3 木糖的提取工艺
半纤维素以β-1,4糖苷键连接,分支度高,能被热的无机酸所水解。利用半纤维素酸催化水解制备木糖的过程较为复杂,其中的反应过程包括:首先,半纤维素苷键在酸性介质中会被裂开而使半纤维素发生降解,半纤维素在酸催化作用下被水解成木糖母液,水解反应如下:
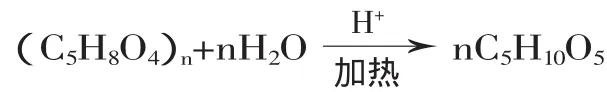
其次,木糖在酸性条件下发生副反应,进一步水解而生成糠醛,水解反应如下:
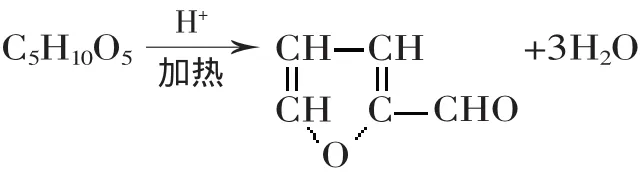
目前,国内外制备木糖的方法有中和法脱酸工艺、离子交换脱酸工艺、酸碱水解法、电渗析脱酸法、酶化学法、层析分离法以及气爆法等。其中,中和脱酸工艺与离子交换脱酸工艺是国内比较成熟的两种制备木糖的工艺方法。
3.1 中和脱酸工艺
中和脱酸法制备木糖的工艺为:原料预处理,水解,中和脱色,离子交换除杂,浓缩结晶,最后分离得到木糖晶体。其中,原料预处理除去了原料中的胶质、果胶、灰分等;中和工序主要是除去水解液中的无机酸;脱色除杂工序包括了使用活性炭和离子交换树脂,该工序可以除去木糖母液中的色素与部分杂质;浓缩结晶工序通过蒸发水解液中微量的有机酸分,控制浓缩后木糖液的浓度与结晶时间得到木糖晶体。
张宏喜[5]等以棉杆为原料,通过中和、脱色、离子交换和结晶等过程,得到纯度为98.5%的木糖晶体。通过单因素多水平实验和正交实验,考察了影响半纤维素水解的因素。研究结果表明,水解的最佳条件为:水解温度140℃,水解时间2.5h,硫酸浓度为5%,固液比为1∶6,木糖的最终产率为11.62%。李雪雁[6]探讨了用酸法从玉米芯中提取木糖的工艺。得出最佳水解条件为:硫酸浓度为1.5%,水解温度100℃,水解时间4h;最佳中和条件为pH=3.0,80℃,中和时间90min;最佳脱色条件为:活性炭用量2%,脱色温度70℃,脱色时间40min。并对离子交换条件进行改进,最终得到的木糖固形物的产率达18%~21%。Silvio S[7]等选用桉树皮为原料,得出最佳水解条件为硫酸浓度5%,温度为140℃,水解10min。常雅宁[8]研究了以竹屑为原料进行水解生产木糖。研究结果表明:硫酸浓度为1.5%,水解温度110℃,水解时间4h,再经过液体量的2%活性炭脱色,用2%热氨水洗涤后的糖液,经过减压蒸馏得到产品。李浩洋[9]研究了稻壳联产二氧化硅和木糖的工艺,所得木糖纯度可达98%。
中和脱酸工艺作为传统的木糖提取工艺,其工艺酸碱消耗低,可降低成本,设备较简单,易操作,投资少。但由于中和工序中形成的石膏(CaSO4)会部分沉积在蒸发器的管壁上,形成隔热层,降低蒸发效率,降低设备使用寿命,且清理麻烦,劳动强度大。
3.2 离子交换脱酸法
针对中和脱酸工艺中的结垢问题,提出了离子交换脱酸工艺。该法是利用木糖在碱性条件下极不稳定的还原性,主要通过离子交换除杂来制备木糖。离子交换脱酸的工艺为:原料预处理,水解,脱色,离子交换除杂,浓缩结晶,最后分离得到木糖晶体。
严浪[10]研究了莲藕渣中多糖的提取和分离,利用离子交换柱层析法分离纯化出莲藕多糖NPh1和NPh2,并用凝胶过滤柱色谱及高效液相色谱仪检测多糖纯度,证明NPh2为纯品,是一种酸性杂多糖,单糖组成为半乳糖、阿拉伯糖、鼠李糖、葡萄糖、岩藻糖和木糖,摩尔比依次为:26.74∶16.17∶5.69∶5.49∶2.31∶1。王丽丽[11]等人选用毛竹为原料,利用阴阳离子交换脱酸法来制备木糖晶体。通过正交设计法,探讨了预水解及水解温度、时间和酸浓度等对水解的影响,得出在水解温度为120℃,时间为2h,硫酸的浓度为2%的最佳的实验条件下,可以得到熔点为140.5~146.0℃、产率为13.4%、纯度为91.3%的木糖晶体。Lavarack[12]等人利用离子交换法研究了从甘蔗渣中提取木糖,得出在120℃,酸浓度在1%,水解时间为2h的实验条件下,可以得到22%的木糖得率。赵先芝[13]选用玉米芯为原料,通过两道离子交换工序,制备在木糖液中产率达到49.67%的白色粉状结晶木糖。贺东海[14]研究了四种不同强碱性阴离子交换树脂MA5133、D296、KD890、D293在木糖除杂中的应用效果。结果表明,KD890交换量大,而且木糖异构化最小,纯度降低最少,是用于木糖净化最理想的三次离子交换树脂。针对离子交换树脂在使用一段时间后,其工作交换量明显降低,而且脱色性能下降的问题,王关斌[15]研究了木糖除杂中广泛应用的D301树脂的再生问题,提出用8%NaOH再生,用HCl浸泡处理树脂铁中毒,延长了树脂使用寿命,提高了离子交换树脂的利用率。王关斌[16]针对在强碱离子交换柱中,木糖分子容易被部分催化异构转化为阿拉伯糖,使得木糖纯度下降,结晶困难的问题,考察了强碱树脂再生浓度、淋洗终点pH、交换温度以及流速对木糖分子异构的影响,得出最佳的交换工艺条件:再生剂浓度为2%、淋洗终点pH为7.5、交换温度20℃、流速为1BV/h。
离子交换脱酸工艺较中和脱酸工艺复杂,树脂用量较多,设备也繁杂,投资大,酸碱消耗多。1992年,山东禹城木糖厂以阳离子交换树脂作为催化剂,生产规模为300t/a。70年代末到80年代初我国在漳州、开化建厂,现已有两条生产工艺,规模已达到2000t/a。1994年起,安徽省科苑应用技术开发(集团)股份有限公司开始从事木糖的研制和生产工作,经过多年努力,现已探索出一条工艺先进、设备简单、操作方便的路线。该路线改进了离子交换工艺,选用了新型结晶方式,产品经过齐鲁石化研究所测试,质量稳定,产品的各项指标均符合美国食品级FCCⅣ版和英国药典BP93版的标准,且保质期可达两年以上。
3.3 酸碱水解法
酸碱水解法也是木糖生产中的常用方法。由于木糖能够溶于碱,并与强碱作用而导致异构化,因而木糖生产中碱法水解不常用。酸水解法工艺简单,容易控制,有利后续分离纯化,是目前工业化制备木糖常用的一种方法。朱琴[17]利用酸水解获取油茶籽壳中木糖,通过正交实验对水解工艺参数进行优化,得到较佳水解条件:水解温度120℃、料液比1∶5、水解时间2h,H2SO42%,木糖得率为9.11%。刘仁成[18]利用椰壳常压酸水解制备木糖,通过正交实验考察了酸预处理时间、酸浓度、椰壳粉粒度、水解时间等对木糖产率的影响。研究表明:用0.2mol/L的盐酸,100℃水解6h,木糖产率可达椰壳空气干燥基质量的16%,水解液经脱色脱盐等一系列工艺制备的椰壳木糖纯度达99%以上。吴真[19]研究了甲酸/盐酸体系水解麦草产生木糖的工艺,发现采用甲酸/盐酸水解体系能有效水解麦草中的半纤维素,含HCl 10%的水解体系在65℃水解麦草0.5h可实现麦草中聚戊糖的充分水解,木糖的得率达到98%。考虑到高温水解的大量能耗和复杂工艺,石荣铭[20]研究了常温酸水解法从稻壳中提取木糖,将半纤维素长时间浸泡浓硫酸,研究结果表明:硫酸浓度为70%,浸泡时间为14h,木糖的得率最高为52.34%。出糖率较高温酸解法有很大的提高,而且摒弃了水解过程中需要的大量能耗,节约了成本,简化了工艺。
3.4 木糖制备的其它工艺
木糖制备的工艺除了中和脱酸、离子交换脱酸和酸碱水解法外,还包括酶化学法[17,21]、电渗析脱酸法[22]、层析分离法[23]、气爆法[24]和结晶木糖法[25]等。
采用酸碱水解法获取木糖虽然转化率较高,但水解过程需要消耗大量的酸碱且对环境造成二次污染,高温高压条件比较苛刻,成本较高且工艺复杂。利用微生物发酵生产木糖及相关产品,副产物少且含量低,易于分离提纯,已经成为世界研究的一个热点。木聚糖的降解需要木聚糖水解酶系中各种酶相互之间协同完成,其中木聚糖酶是最关键的水解酶。目前对木聚糖酶的研究集中于真菌和细菌产生的木聚糖酶,它只含一个亚单位的蛋白质。多数木聚糖酶作用的稳定pH范围为3.0~10.0,最适pH范围为4.0~7.0,最适作用温度为40~60℃[26]。
朱琴[17]利用微生物发酵获取油茶籽壳中木糖的研究中,研究了白腐菌微生物发酵获取油茶籽中的木糖。采用响应面法对液体培养基组成优化:油茶籽壳4%,(NH4)SO4(W/V)1%、MgSO4·7H2O(W/V)0.6%。经用此配方组成的培养基进行发酵实验验证,其木糖实际得率为2.89%。通过摇瓶发酵实验得到了较合理的液体培养条件:培养液初始pH5.5、装液量为100mL/250mL、接种量10%、培养温度30℃、培养时间48h、摇床转速120r/min。按此液体培养条件摇瓶发酵后,木糖得率为2.96%。刘长虹[21]用碱法从玉米秸秆中提取木聚糖,再利用木聚糖酶酶解木聚糖制备木糖。结果表明:粉碎过的玉米秸秆经过沸水浸4h,过滤,用10%NaOH溶液按m(秸秆)∶m(NaOH溶液)为1∶15,于80℃下浸提2h,木聚糖提取率可达30%。取50mL木聚糖液,加入20mL木聚糖酶液,在水解温度65℃下反应5h,最后测得木糖的得率为20.34%。
化学转化生产木糖及相关产品存在着工艺设备要求高,副产物成分复杂,化学试剂用量大,污染严重等问题。有学者在此基础上提出了气爆法提取木糖。崔素芬[24]研究了蒸汽爆碎处理甘蔗叶提取木糖过程中爆碎压力、维压时间对木糖溶出量的影响。研究表明:木糖溶出量随爆碎压力增加而增加,随维压时间增加,先增大后减小,随粒度增大而减小,随固液比增大先减小后增大。崔素芬采用响应面实验和DesignExpert 7.0软件分析实验设计拟合得到的模型较好地符合实际,并得到最佳爆碎工艺为:爆碎压力1.1MPa,维压时间12.5min,粒度100目,液料比15∶1(v/w)。
此外,还发展了电渗析脱酸工艺及层析分离工艺。电渗析脱酸法尚处于实验阶段,世界上还没有工业化生产。电渗析法的工艺为:原料经预处理、水解、脱色、电渗析、浓缩结晶,最后分离得到木糖晶体。由于电渗析的效果不是很理想,一般只能达到80%的渗析效果[22],故目前还没有研究者对此工艺进行深入研究。层析分离制备木糖工艺是当今世界较先进的生产方法,采用连续水解工艺,提高了木糖产率,水解液糖浓度高达10%以上[23]。层析分离法的工艺为:原料经预处理、水解、中和、脱色、离子交换、蒸发、木糖层析分离、浓缩结晶,最后分离得到木糖晶体。采用层析分离技术使产品纯度提高,质量好,同时降低能耗,国内该工艺尚未达到工业化生产水平。结晶木糖法工艺较简单,但总产率不高是该法的主要缺陷。胡德荣[25]利用结晶木糖法,以稻壳为原料,得到收率为5%的木糖晶体。
4 木糖检测方法的研究进展
2006年11月25日,中国发酵工业协会在北京召开《木糖国家标准》编写预备会,会上提出了木糖作为一种食品、饮料等的重要添加剂有其特殊性。因此对木糖的纯度等相关指标提出了更高的要求,这对木糖检测和分析方法也提出了更高的要求。目前,木糖定性定量分析方法主要有费林试剂法[3]、3,5-二硝基水杨酸法(又称DNS法)[27-28]、薄层层析法[29]、Douglas法[30-31]和色谱法[32-33]等。
4.1 DNS法和费林试剂法
DNS法和费林试剂法统称还原法,是根据木糖是一种还原糖的特性来进行测定。DNS法其原理是3,5-二硝基水杨酸溶液与还原糖溶液共热后被还原成棕红色的氨基化合物,在一定实验范围内还原糖的量和棕红色物质颜色深浅的程度成一定比例关系,可用比色测定。在NaOH和丙三醇存在下,3,5-二硝基水杨酸(DNS)与还原糖共热后被还原生成氨基化合物(式1),在过量的NaOH碱性溶液中此化合物呈桔红色,在一定波长处有最大吸收,其吸光度与还原糖含量有线性关系。资料显示,采用DNS法的测定最佳波长有480nm[27]和490nm[28]两种说法。费林试剂法原理是:费林氏A、B液混合时,生成天蓝色氢氧化铜沉淀,该沉淀立即与酒石酸钾钠反应,生成深蓝色的络合物——酒石酸钾钠铜。当酒石酸钾钠铜与木糖混合在一起时,该络合物被木糖还原,生成红色的氧化亚铜沉淀(式2)。还原法操作简便、快速,杂质干扰较少。

4.2 薄层层析法
薄层层析法是一种固-液吸附色谱,是近年来发展起来的一种微量、快速而简单的色谱法,它兼备了柱色谱和纸色谱的优点,此法特别适用于检测挥发性较小或较高温度易发生变化而不能用气相色谱分析的物质。具体操作过程可分为:调浆、涂板、活化、点样分析。在干净的玻板(10×3cm左右)上均匀地涂一层吸附剂或支持剂,待干燥、活化后将D-木糖标准液溶液用管口平整的毛细管滴加于离薄层板一端约1cm处的起点线上,晾干或吹干后置薄层板于盛有展开剂的展开槽内,浸入深度为0.5cm。待展开剂前沿离顶端约1cm附近时,将色谱板取出,干燥后喷以显色剂,或在紫外灯下显色。
4.3 Douglas法
因木糖是戊糖类中的一种,具备戊糖的通性。Douglas法其原理是利用抽提试剂在高温条件下将待测样品中的戊聚糖水解为木糖和阿拉伯糖,间苯三酚选择性的与戊糖发生显色反应,并且显色物质浓度与吸光度呈正相关关系,从而反映出原试样中戊糖的浓度。资料显示,Douglas法测定有单波长(552nm)[30],也有双波长(552~510nm)[31]之说。
4.4 色谱法
色谱法分为气相色谱法、液相色谱法和离子色谱法等。气相色谱法具有分离效率高、分析速度快、样品用量少、检测灵敏度高等优点。但对于木糖这类挥发性和热稳定性较低的物质,需先将木糖通过硅烷化法和乙酰化法制成相应的低沸点衍生物,然后进行测试。目前该方法已成功用于海洋胶体中的木糖含量测定(YY-SW-TL-0493)和南瓜中木糖含量的测定(YY-SW-TL-0486),但气相色谱法操作中样品处理复杂、操作费时、误差较大,因而有一定的局限性。传统的液相色谱采用柱后衍生和可见光检测,在用于木糖测定时,需将样品制备成具有紫外吸收或能发出荧光的衍生物,制备过程复杂。现在普遍应用的是高效液相色谱法(HPLC),它是采用高压输液系统,将具有不同极性的单一溶剂或不同比例的混合溶剂、缓冲液等流动相泵入装有固定相的色谱柱,在柱内各成分被分离后,进入检测器进行检测,从而实现对试样的分析。在进行糖分分析时,填充材料的选择是否恰当是色谱纯化分离的关键所在,常选择氧化铝、活性炭、离子交换剂等作为分离介质。近年来也有报道采用[32]氨基柱和Waters-Sugar-PakTM1[33]。离子色谱法是一种改进的色谱分析方法,用高效的阴离子交换柱分离糖,用脉冲积分安培检测器进行检测。离子色谱柱可直接进行低浓度木糖的定量分析,无需衍生和样品前处理,既节约了时间,也避免了一些有毒衍生试剂的使用。分析木糖常用的交换柱有CarboPacPA10等。直流安培检测器不能用于糖的检测,主要是因为糖氧化会对电极产生不可逆的污染,而PAD检测器解决了这一问题,并具有很高的灵敏度。
5 结论
木糖作为一种新型的添加剂和甜味剂,产品用途较广,功能价值较高,已越来越广泛地应用到人们日常生活中。然而,在工业化应用的工艺中,木糖得率较低以及木糖结晶后的母液中具有较高含量的糖分等缺陷仍未得到根本的改善。我国拥有得天独厚的原材料资源,拥有广阔的发展天地和市场前景。如何变废为宝,降低成本,改善工艺,是广大科技工作者需要解决的问题。
[1]尤新,朱路甲.无热量甜味料-结晶木糖的性质功能和应用前景[J].中国食品添加剂,2009(1):52-56.
[2]邬义明.植物纤维化学[M].北京:中国轻工业出版社,1997.
[3]黄诚.从稻壳中提取木糖研究[D].重庆:重庆大学硕士学位论文,2007.
[4]石波,李里特.低聚木糖的制备与分离[J].食品添加剂,2004,25(7):113-114.
[5]张宏喜,赵秀峰,魏玲,等.棉杆水解制备木糖的研究[J].安徽农业科学,2010,38(23):12687-12689.
[6]李雪雁,王丹,胡朝霞,等.玉米芯酸法提取木糖的工艺改进[J].食品工业科技,2009,30(6):263-264,308.
[7]Silvio S Silva,Maria G A Felipe,Felipe Joao B A,et al.Acid Hydrolysis of Eucalyptus grandis chips for microbial production of xylitol[J].Process Biochemistry,1998,33(1):63-67.
[8]常雅宁,颜淑玮,俞建瑛,等.竹屑制备木糖的工艺研究[J].林产化学与工业,2005,25(2):52-54.
[9]李浩洋,汪海滨.从稻壳中提取二氧化硅和木糖的工艺研究[J].广东化工,2007,34(11):43-45.
[10]严浪,张树明,张凡华,等.莲藕渣中多糖的提取及性质初步研究[J].食品科学,2007,28(12):226-230.
[11]王丽丽,莫卫民,卢耀平,等.毛竹水解制取木糖[J].浙江化工,1996,27(2):27-31.
[12]Lavarack B P,Griffin G J,Rodman.The acid hydrolysis of sugarcane bagasse hemicellulose to produce xylose,arabinose,glucose and product[J].Biomass and Bioenergy,2002,23:367-380.
[13]赵先芝.结晶木糖研制[J].河南化工,2001(10):8-9.
[14]贺东海,赵光辉,王关斌,等.用于木糖净化的三次离子交换树脂的选择[J].应用化工,2005,34(6):375-376.
[15]王关斌,赵光辉,贺东海,等.木糖精制中D301树脂污染及处理[J].天津化工,2005,19(6):42,57.
[16]王关斌,赵光辉,贺东海.强碱树脂在木糖应用中存在的问题及解决方法[J].河北化工,2005(2):49-50.
[17]朱琴.利用酸水解和微生物发酵获取油茶籽壳中木糖的研究[D].郑州:河南农业大学硕士学位论文,2008.
[18]刘仁成,黄广民,姚伯元,等.椰壳常压酸水解制备木糖[J].食品科学,2006,27(12):263-267.
[19]吴真,林鹿,孙勇,等.甲酸/盐酸体系水解麦草产生木糖的研究[J].食品科技,2008(2):90-93.
[20]石荣铭,梁莉丽.常温酸水解法从稻壳中提取木糖的研究[J].食品科技,2007(12):212-214.
[21]刘长虹,吴树新.酶催化法制备木糖的研究[J].化工科技市场,2010(12):39-41,58.
[22]Nomura Y,Hallsworth J E,Iwahara M,et al.Rapid and efficient production of L-lactate from xylose using electrodialysis culture-associated product separation[J].World Journal of Microbiology and Biotechnology,1998(6):911-916.
[23]Lasrson M,Sundberg R,Folestad S.On-line capillary electrophoresis with mass spectrometry detection for the analysis of carbohydrates after derivatization with 8-aminonaphthalene-1,3,6 trisulfonic acid[J].J Chromatogr A,2001,934:75-85.
[24]崔素芬,李坚斌,杭方学,等.蒸汽爆碎处理甘蔗叶提取木糖的研究[J].食品工业科技,2010,31(1):217-219.
[25]胡德荣,丁辰元,张新位,等.从稻壳中提取木糖[J].首都师范大学学报:自然科学版,1995,16(1):68.
[26]Kulkartui N,Shend Y E A,Rao M.Molecular and biotechnological aspects of xylanase[J].FEMS Microbiol Rev,1999(23);444-456.
[27]曾莹,钟晓凌,夏服宝.木聚糖酶活力测定条件研究[J].生物技术,2003,13(5):21-22.
[28]陆文清,刘伟,刘兴海,等.几种常见饲用酶制剂的酶活测定与分析[J].饲料工业,2001,21(2):17-20.
[29]Liao Wei,Liu Chuanbin,Chen Shualin.Optimizing dilute acid hydrolysis of hemicellulose in a nitrogen-rich cellulosic material-dairy manure[J].Bioresourse Technology,2004,94:33-41.
[30]郑学玲.小麦鼓皮戊聚糖的分离制备,理化性质及功能特性研究[D].无锡:江南大学硕士论文,2002.
[31]时侠清.间苯三酚分光光度法测定小麦戊聚糖新方法及其应用[J].安徽技术师范学院报,2005,19(3):6-10.
[32]方宏,曾健智,张厚瑞.高效液相色谱法检测发酵液中木糖和木糖醇[J].广西植物,2004,24(3):275-277.
[33]杨俊,王文辉,陈益民.高效液相色谱法快速分析木糖及木糖醇[J].昆明大学学报:综合版,2000(2):60-61.
Research progress in preparation processing and detection method of xylose
FU Wen,WANG Li*,SHI Bo
(College of Chemical and Environmental Engineering,Guangdong University of Petrochemical Technology,Maoming 525000,China)
Xylose as an important chemical raw materials,has been widely used in food,beverage and other industries.This paper reviewed the progress in the preparation process of xylose.The detection method of xylose was also described simply.
xylose;technology;review
TS201.1
A
1002-0306(2012)05-0405-05
2011-04-19 *通讯联系人
付文(1983-),男,硕士,讲师,研究方向:生物质综合利用。
广东省自然科学基金(S2011040001765);广东石油化工学院大学生创新实验项目。
