脉冲放电等离子体制备壳聚糖铁(Ⅲ)配合物及结构表征
2012-10-25马凤鸣王振宇
马凤鸣,王振宇,*
(1.哈尔滨工业大学食品科学与工程学院,黑龙江哈尔滨 150090;
2.东北林业大学林学院,黑龙江哈尔滨 150040)
脉冲放电等离子体制备壳聚糖铁(Ⅲ)配合物及结构表征
马凤鸣1,2,王振宇1,2,*
(1.哈尔滨工业大学食品科学与工程学院,黑龙江哈尔滨 150090;
2.东北林业大学林学院,黑龙江哈尔滨 150040)
以壳聚糖浓度、Fe3+浓度、极板间距和处理时间为影响因素,采用脉冲放电等离子体法制备壳聚糖(CTS)铁(Ⅲ)配合物。并利用红外光谱法(FT-IR)和紫外光谱(UV)进行结构表征。实验结果表明,脉冲放电等离子体可以用来制备CTS-Fe3+配合物,Fe3+浓度、处理时间与吸附量成正相关关系,随影响因素值增大,吸附量增大;壳聚糖浓度、极板间距成负相关关系,随影响因素值降低,吸附量减少。壳聚糖与铁(Ⅲ)发生配位作用的基团可能是-NH2和-COOH。
壳聚糖,脉冲放电,等离子体,铁(Ⅲ)配合物,表征
壳聚糖是一种从虾、蟹等甲壳纲动物外壳中提取的一种可再生、无毒副作用的天然高分子多糖,具有抑菌、增强免疫力、降血脂、抗癌等药理活性[1-3]。由于壳聚糖分子链中含有大量羟基、氨基及N-乙酰氨基,使壳聚糖及其衍生物能有效地捕集或吸附溶液中的金属离子,是金属离子的良好配体。因此,壳聚糖可以与过渡及稀土金属离子进行配位形成金属配合物,改善其物理化学性质和生物活性,从而使其在废水处理、食品、化工、农业、生物工程和医药等方面得到了广泛的应用[4-7]。目前,合成金属配合物的传统方法是水浴加热合成,需几小时至十几小时的反应,处理时间太长,探索一种高效的处理方法成为必要。因此,一些辅助方法被应用到金属配合物的合成,如微波法、超声波、磁场等[8-10]。脉冲放电等离子体技术是一种综合了脉冲电场(PEF)、脉冲紫外(PUV)、臭氧处理(OT)、脉冲电晕处理(PCT)各个效应的处理技术[11]。在处理过程中会产生光子、电子、正负离子、基态或激发态原子、活性自由基、射线以及多种氧化性物种。这些氧化性自由基和氧化性分子均具有较高的氧化电位,可以有效地氧化降解有机物分子。同时,在水溶液中还形成的高温热解、超声波和紫外光效应等[11-15]。本文认为脉冲放电等离子体技术通过其降解作用,可能会打断壳聚糖的高分子链,降低其分子量,使壳聚糖的脱乙酰度增加、高分子链上的配合位点增多,以此提高壳聚糖的配合量,同时产生的热效应也能提高配合反应的速率。因此,将等离子体应用于壳聚糖金属配合物的合成具有一定的可行性。因此,本文采用脉冲放电等离子体技术,将壳聚糖与Fe3+化合物反应,合成了CTS-Fe3+配合物,并采用红外光谱和紫外光谱进行结构表征,确认脉冲放电等离子体制备CTS-Fe3+配合物的可行性,为脉冲放电等离子体应用于壳聚糖金属配合物的合成提供一定的科学依据,为制备壳聚糖配合物开辟新的强化途径。
1 材料与方法
1.1 材料与仪器
壳聚糖 国药集团化学试剂有限公司;乙酸、硫酸铁铵、硫酸、氨水、乙酸钠、邻菲罗啉、盐酸羟胺、无水乙醇 均为分析纯;所用其他试剂 均为分析纯。
T6紫外可见分光光度计 北京普析通用公司;JHS-1电子恒速搅拌器 杭州仪表电机厂;TDL-5台式离心机 上海科兴仪器有限公司;FD-1真空冷冻干燥机 北京博医康实验仪器有限公司;YP200lN电子天平 上海精天电子仪器厂;PB-10 pH计 赛多利斯科学仪器(北京有限公司);脉冲放电等离子体处理系统 哈尔滨工业大学自制(见图1),电感脉冲放电电路,脉冲功率为350W,脉冲电压为60kV,不锈钢针-板电极,极板间距为1~6mm可调。

图1 脉冲放电等离子体处理系统Fig.1 Pulsed discharge plasma treating system
1.2 实验方法
1.2.1 脉冲放电等离子体法制备CTS-Fe3+配合物称取一定量壳聚糖,溶于1%HAc中,配制成一定浓度壳聚糖溶液。缓慢滴加一定浓度的Fe3+溶液,调pH至1.6~1.8。将混合溶液倒入脉冲放电等离子发生装置中进行处理,处理后溶液加入3倍量的无水乙醇,离心,取沉淀,洗涤。以无水乙醇洗涤数次至无Fe3+检出,于真空冷冻干燥机中干燥得到CTS-Fe3+配合物产品。
1.2.2 化学法制备CTS-Fe3+配合物 处理方式同1.2.1,壳聚糖浓度为10mg/m L,Fe3+浓度为0.5mg/m L,在电动搅拌条件下将硫酸铁铵水溶液缓慢滴加到壳聚糖醋酸溶液中,反应5h。并在相同条件下,与脉冲放电等离子体条件下处理1.5h进行对比实验研究。
1.2.3 Fe3+含量的测定[16]壳聚糖与Fe3+形成配合物沉淀后,经离心过滤,准确吸取上清液1m L置于50m L容量瓶,然后分别加入1m L 10%盐酸羟胺、5m L 1mol/L NaAc、2m L 0.15%邻二氮菲,每加一种试剂后摇匀,静置10m in。用分光光度计在510nm波长处测定各样品的吸光度,并通过标准曲线求出各样品中铁的含量。根据处理前后溶液中Fe3+浓度的变化,按下式计算其吸附量:

式中,Q为吸附量(mg/g);V为Fe3+溶液的体积(m L);C0、C分别为处理前后溶液中Fe3+的浓度(mg/m L);M为壳聚糖的质量(g)
1.2.4 CTS-Fe3+配合物的表征
1.2.4.1 红外吸收光谱测定 采用KBr压片法测定壳聚糖、脉冲放电等离子体制备CTS-Fe3+配合物的红外吸收光谱,扫描波数范围为400~4000cm-1。
1.2.4.2 紫外吸收光谱测定 分别以1%醋酸为试剂空白,于200~400nm波长范围内测定壳聚糖、脉冲放电等离子体制备CTS-Fe3+配合物的紫外吸收光谱。
2 结果与分析
2.1 脉冲放电等离子体法制备CTS-Fe3+配合物实验研究
2.1.1 Fe3+浓度对吸附量的影响 以极板间距2mm,壳聚糖浓度10mg/m L,Fe3+浓度为0.2、0.4、0.6mg/m L,进行脉冲放电等离子体法制备CTS-Fe3+配合物实验研究。

图2 Fe3+浓度对吸附量的影响Fig.2 Effect of Fe3+concentration on adsorption capacity
由图2可知,吸附量与Fe3+浓度成正比。处理时间小于75m in时,吸附量迅速增加,配位能力较强。75m in时,Fe3+浓度为0.2、0.4、0.6mg/m L条件下的吸附量分别为:10.74、25.64、49.04 mg/g。大于75m in后,曲线趋于平缓,90min时吸附量趋于最大值。此时。吸附量分别为12.05、25.9、50.06 mg/g。
2.1.2 壳聚糖浓度对吸附量的影响 以极板间距2mm,Fe3+浓度0.6mg/m L,壳聚糖浓度4、8、12mg/m L,进行脉冲放电等离子体法制备CTS-Fe3+配合物实验研究。

图3 壳聚糖浓度对吸附量的影响Fig.3 Effectof chitosan concentration on adsorption capacity
由图3可知,吸附量与壳聚糖浓度成反比。这与王孝平等[17]的研究结果相符。处理时间大于60min时,12、8mg/m L浓度的壳聚糖的吸附量均趋于平缓,而4mg/m L的壳聚糖浓度条件下,吸附量仍迅速上升。90m in时均趋于最大值。此时壳聚糖浓度为4、8、12mg/m L组别的吸附量分别为69.79、47.52、29.77mg/g。
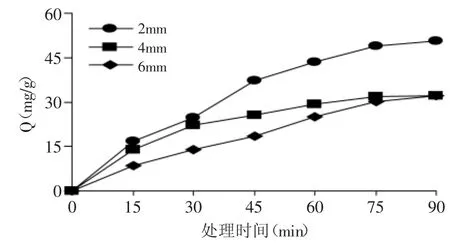
图4 极板间距对吸附量的影响Fig.4 E ffectof the distance between the electrodes on adsorption capacity
2.1.3 极板间距对吸附量的影响 以Fe3+浓度0.6mg/m L,壳聚糖浓度10mg/m L,极板间距为2、4、6mm,进行脉冲放电等离子体法制备CTS-Fe3+配合物实验研究。由图4可知,吸附量与极板间距成反比。处理时间大于75m in时,三个浓度的壳聚糖的吸附量均趋于平缓,90m in时趋于最大值。此时极板间距为2、4、6mm组别的吸附量分别为50.61、32.24、32.1mg/g。极板间距2mm的配位能力要显著高于4、6mm。
2.1.4 传统化学法和脉冲放电等离子体法比较结果分析 由表1可知,在同样的壳聚糖浓度和Fe3+浓度前提条件下,化学方法制备CTS-Fe3+配合物需搅拌反应5h,脉冲放电等离子体法制备CTS-Fe3+配合物只需1.5h;化学法处理条件下,吸附量为23.00mg/g;而脉冲放电等离子体法条件下,吸附量为40.09mg/g。

表1 等离子法和传统化学法比较分析Table 1 Result of comparison experiment
综上所述,与化学法相比较,脉冲放电等离子体法制备CTS-Fe3+配合物具有处理时间短、效率高等优点。
2.2 CTS-Fe3+配合物表征分析
2.2.1 红外光谱分析(FT-IR) 壳聚糖及CTS-Fe3+配合物的红外光谱如图5所示。配位反应后壳聚糖原位于3432cm-1处的氨基及羟基的重叠峰(分别为N-H和O-H的伸缩振动吸收峰)移至3422cm-1,且吸收峰变宽,说明壳聚糖中的-NH2、-OH可能参与了配位反应;在1522cm-1处(-NH2的伸缩振动吸收峰)产生了一个新的吸收峰,进一步说明壳聚糖中的-NH2参与了配位反应;原位于1593cm-1处的乙酰氨基的C=O伸缩振动吸收峰向低频移至1636cm-1处,说明壳聚糖中极少量的乙酰氨基也可能参与了配位反应[7,18-19]。

图5 壳聚糖(a)和CTS-Fe3+配合物(b)的红外光谱Fig.5 Infrared spectra of CTSand CTS-Fe3+complex
2.2.2 紫外光谱分析(UV) 壳聚糖及其CTS-Fe3+配合物的紫外吸收光谱如图6所示。结果表明,壳聚糖样品仅在205nm处有1个强吸收峰且峰形较窄,而CTS-Fe3+配合物除在205nm处有一个宽而强的吸收峰外,还在334nm处产生新的吸收峰,这可能是配合物中氮、氧的孤对电子发生n→σ*跃迁,导致电子光谱发生的变化[20]。由此可证明,Fe3+与壳聚糖发生了配位反应,且C-N键由于-NH2与Fe3+的结合,在一定程度上使该键有所削弱,从而可推断-NH2是壳聚糖分子中主要吸附部位[21]。

图6 壳聚糖和不同处理时间下CTS-Fe3+配合物的紫外光谱Fig.6 UV spectra of CTSand CTS-Fe3+complex at different treatment time
3 结论
3.1 以壳聚糖浓度、Fe3+浓度、极板间距为影响因素进行制备CTS-Fe3+配合物实验研究,结果表明,Fe3+浓度、处理时间与吸附量成正相关关系,随影响因素值增大,吸附量增大;壳聚糖浓度、极板间距成负相关关系,随影响因素值降低,吸附量减少。
3.2 与传统化学法相比,脉冲放电等离子体法具有吸附量更高,处理时间短的优点。
3.3 红外光谱和紫外吸收光谱显示壳聚糖中的-NH2可能参与了与Fe3+离子的配位反应。另外,极少量的乙酰氨基也可能参与了配位反应。
[1]张新娜,孙君社,王淑豪,等.羧甲基壳聚糖亚铁配合物的表征及其对CO的吸附研究[J].高校化学工程学报,2011,25(1):91-95.
[2]张宏绪.壳聚糖及其与金属离子配合物的应用[J].世界元素医学,2007,14(1、2):8-11.
[3]凌沛学,荣晓花,张天民.壳聚糖及其衍生物的医药研究进展[J].食品与药品,2008,10(9):69-71.
[4]冯小强,李小芳,杨声,等.壳聚糖Fe(Ⅲ)配合物的合成、表征及抑菌性能[J].天然产物研究与开发,2009,21:922-925,938.
[5]李树全.壳聚糖类金属配合物的合成及应用[J].河北化工,2011,34(1):32-36.
[6]沈少飞,叶盛权,吴晖,等.羟丙基壳聚糖亚铁配合物的合成[J].食品工业科技,2011,32(3):242-246.
[7]冯小强,李小芳,杨声,等.壳聚糖镧配合物的制备_表征及其抑菌性能[J].食品工业科技,2010,31(2):304-310.
[8]蒋寅,王兆梅,叶盛权,等.外加物理场对壳聚糖-亚铁配合反应的影响[J].华南理工大学学报:自然科学版,2008,36(7):62-66.
[9]曹佐英,葛华才,赖声礼.微波能促进壳聚糖钙离子配合物的制备研究[J].食品工业科技,2000,21(2):11-13.
[10]曹佐英,赖声礼.微波辐射下壳聚糖Zn(Ⅱ)配合物的合成[J].现代化工,1999,19(11):24-27.
[11]Marsilia L,Espieb S,Andersona JG,etal.Plasma inactivation of food-related microorganisms in liquids[J].Radiation Physics and Chemistry,2002,65:507-513.
[12]Moreau M,Orange N,Feuilloley M G J.Non-thermal plasma technologies:New tools for biodecontamination[J].Biotechnology Advances,2008,26:610-617.
[13]李雁晖,林向阳,张宏,等.非热等离子体杀菌技术研究进展[J].农产品加工·学刊,2008,145(8):34-36.
[14]Tendero C,Tixier C,Tristant P,et al.Atmospheric pressure plasmas:A review[J].Spectrochimica Acta PartB,2006,61:2-30.
[15]王慧娟.脉冲放电等离子体水处理技术及其研究进展[J].安徽农业科学,2009,37(22):10707-10710.
[16]战春玲,王庆宇,李倩男,等.中草药中铁含量的测定与药效分析[J].广东微量元素科学,2007,14(8):25-27.
[17]王孝平,姜皓然,田海燕,等.壳聚糖与羧甲基壳聚糖对铁离子的络合性能研究[J].化学与生物工程,2009,26(3):30-33.
[18]葛欣,高冷,李亚丰,等.壳聚糖铁(Ⅲ)配合物的合成及其对苯酚羟基化的催化性能研究[J].化学与生物工程,2009,26(4):35-38.
[19]孙兰萍,赵大庆,张斌,等.羧甲基壳聚糖铁(Ⅲ)配合物的合成及结构表征[J].食品工业科技,2007,28(11):81-86.
[20]覃彩芹,池伟林,舒海波.壳聚糖的体内生物活性功能研究进展[J].孝感学院学报,2004,24(6):5-9.
[21]许晖,孙兰萍,张胜义,等.壳聚糖铁(Ⅲ)配合物吸附动力学研究[J].食品科学,2007,28(1):63-67.
High voltage pulsed discharge plasma on the coordinated reaction for chitosan-Fe(Ⅲ)and structure characterization
MA Feng-m ing1,2,WANG Zhen-yu1,2,*
(1.School of Food Science and Engineering,Harbin Institute of Technology,Harbin 150090,China;
2.College of Forestry,Northeast Forestry University,Harbin 150040,China)
High voltage pulsed discharge p lasma for synthesis of chitosan(CTS)-Fe3+com p lex was stud ied. Influence factors were chitosan concentration,Fe3+concentration,the d istance between the electrodes and treatment time.The struc ture of the comp lex was characterized by FT-IR,UV.The result showed that Fe3+concentration and treatment time were positive.The higher the Fe3+concentration and treatment time,the greater the adsorp tive capacity.Chitosan concentration and the d istance between the electrodes were negative.The higher the chitosan concentration and the d istance between the elec trodes,the lower the adsorp tive capacity. Fe3+was coord inated w ith-NH2,-COOH.
chitosan;pulsed d ischarge;p lasma;Fe(Ⅲ)com p lex;characterization
TS201.2
A
1002-0306(2012)22-0186-04
2012-05-25 *通讯联系人
马凤鸣(1981-),男,硕士,讲师,主要从事物理技术在食品加工中的应用研究。
