含川芎、当归中成药中藁本内酯的检测分析
2012-07-28汪程远谭月晗
汪程远 张 燕 谭月晗
重庆工商大学药物化学与化学生物学研究中心,重庆 400067
当归、川芎是养血活血的常用传统中药,也是中成药制剂的常用药材。在《中国药典》2005年版一部中[1],仅含当归的中成药制剂有52个品种,仅含川芎的中成药制剂有36个品种,当归和川芎都含有的制剂有47个品种,含有当归、川芎药材的中成药制剂品种在《中国药典》2005年版中数量占23.9%,因而当归、川芎成为了《中国药典》2005年版中用量最广泛的常用药材。现常用阿魏酸和川芎嗪作为当归、川芎的指标检测成分,但实际上当归、川芎中藁本内酯含量远高于阿魏酸和川芎嗪在药材中的含量[2-6]。据文献报道藁本内酯在当归、川芎中分别高达2.689%[7]、1.857%[8],因此藁本内酯为当归、川芎中含量最高的活性成分。已有大量研究报道藁本内酯对心血管系统有较强药理活性[9-11],其可解除血管痉挛、增加冠脉流量、扩张微血管等,这些作用符合当归、川芎活血化瘀的药理功效。因此,将藁本内酯作为含当归、川芎中成药中活性检测成分是最有科学依据的。但由于藁本内酯结构特殊稳定性差[12-13],其藁本内酯对照品制备难,保存更难[14],现还未有文献报道中成药制剂中的藁本内酯检测分析。笔者在用HPLC测定川芎中藁本内酯研究的基础上[8],用自制稳定的藁本内酯对照品建立了藁本内酯的薄层色谱法(TLC)和高效液相色谱(HPLC)检测分析方法,分别对含当归、川芎的代表性中成药制剂中藁本内酯进行定性和定量分析检测,为此类药材复方制剂的分析检测、质量控制和临床治疗用药监测提供参考。
1 仪器与试药
TU-Ⅱ暗箱式紫外观察仪(内置254 nm/366 nm紫外光灯管,上海科哲生化科技有限公司);Agilent 1260型液相色谱仪(带四元泵、自动进样器、UV检测器,安捷伦科技有限公司);超声波清洗仪(SB-5200D,宁波新芝生物科技股份有限公司);梅特勒AG204电子天平;Nikon数码相机(D700,日本尼康公司);Milli-Q纯水仪;Eppendorf 5417C高速离心机。
防风通圣丸(河南省宛西制药股份有限公司,批号:100401);妙济丸(陕西利君现代中药有限公司,批号:100803);心通口服液(鲁南厚普制药有限公司,批号:10062007);天麻丸(重庆桐君阁药厂有限公司,批号:10070002);十全大补丸(重庆中药二厂,批号:1002001);黄氏响声丸(无锡济民药业股份有限公司,批号:110616);木瓜片(吉林亚泰明星制药有限公司,批号:20101101);止痛化癥片(江西杏林白马药业有限公司,批号:20100706);石斛夜光丸(长春人民药业集团有限公司,批号:111207);川芎茶调浓缩丸(重庆中药二厂有限公司,批号:1012026);补肾益脑丸(牡丹江灵泰药业股份有限公司,批号:100802);逍遥丸(江苏康缘药业股份有限公司,批号:091213);黄连上清丸(四川绵阳制药有限公司,批号:55110016);九味羌活丸(四川绵阳制药有限公司,批号:55110042);乌鸡白凤丸(江西民济药业有限公司,批号:100612);人参再造丸(吉林天强制药有限公司,批号:1000901)。甲醇(美国Merck公司)为色谱纯,水为超纯水,其他试剂为分析纯。藁本内酯对照品(自制,经核磁共振氢谱和碳谱鉴定,其纯度以HPLC和GC测定,按面积归一化法计算大于98.0%)。
2 方法与结果
2.1 TLC检测分析
2.1.1 样品溶液制备 取各中成药用研钵研磨成细末状,分别称取2 g各药细末加入10 mL的甲醇溶解,再用超声波清洗机分别超声30 min,离心,取上清液作为供试样品,备用。称取藁本内酯对照品10 mg加入10 mL甲醇溶解,作为对照样品,备用。
2.1.2 色谱条件 以HF254硅胶板为固定相,以石油醚∶乙酸乙酯(10∶1)为展开剂,在层析缸中充分饱和,展开,取出晾干,在TU-Ⅱ暗箱式紫外仪254 nm和365 nm波长下视检,用数码相机照相,记录色谱图。
2.1.3 检测结果 取上述制备好的各供试样品和藁本内酯对照品液,点样于一块长HF254硅胶板上,饱和,展开,记录色谱图,藁本内酯的Rf值为0.52,总色谱见图1。
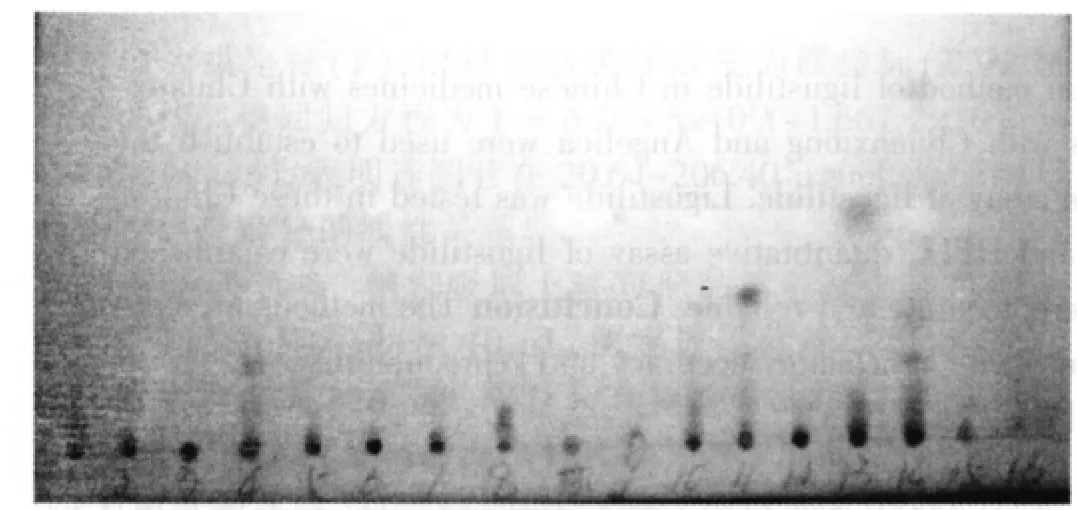
图1 各中成药TLC图谱
从图 1 可看出 2、3、7、8、13、15、16 在藁本内酯对照品点处没有类似的荧光斑点,说明这几个中成药制剂中TLC检测不到当归、川芎的有效成分藁本内酯,可以初步判断这几个制剂中当归、川芎的药材加入量很低或没有加入正品当归、川芎药材。
2.2 HPLC含量检测
2.2.1 对照品溶液制备 精密称取藁本内酯对照品5.3 mg置于50 mL容量瓶中,用甲醇溶解定容,配制成浓度为106 μg/mL标准溶液,备用。
2.2.2 样品溶液制备 取各中成药用研钵研磨成细末状,分别称取2 g各药细末,加入20 mL甲醇,共加两次,超声提取30 min,过滤,滤液置于50 mL容量瓶中,加甲醇定容,得到各样品溶液,备用。
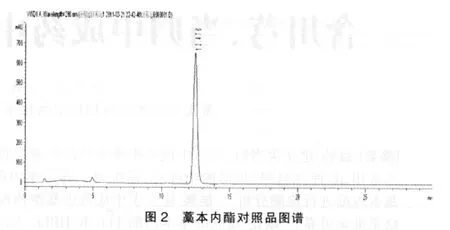
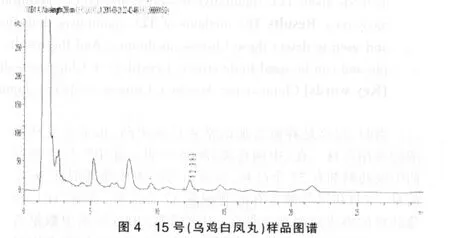
2.2.3 色谱条件[8]Agilent 1260型液相色谱仪(四元泵、自动进样器、UV 检测器);色谱柱:Hypersil ODS(4.6 mm×150 mm,5 μm);流动相:甲醇-5%异丙醇(45∶55);检测波长:280 nm;流速:1 mL/min;柱温:25℃。在此条件下,样品中的藁本内酯与其他峰均能达到基线分离,藁本内酯的保留时间为12.1 min,对照品和样品的色谱见图2~4,其中样品图随机选择11和15号。

2.2.4 标准曲线的制备 精密量取对照品溶液,用流动相稀释制成含藁本内酯 1.06、5.30、10.60、21.20、53.00 μg/mL 的系列溶液。按“2.2.3”项下色谱条件,分别准确进样10 μL,测定,记录各自峰面积。以对照品重量(μg)为横坐标X,以峰面积为纵坐标Y,得藁本内酯线性回归方程为:Y=2485.2X+19.943(r=0.9990,n=5),结果显示,藁本内酯含量在 1.06~53.00 μg/mL线性关系良好。
2.2.5 精密度试验 取同一样品(11号补肾益脑丸)溶液,按上述色谱条件,重复进样10次,每次10 μL,测定藁本内酯峰面积,RSD为0.78%,表明仪器精密度良好。
2.2.6 稳定性考察 取同一样品(11号补肾益脑丸)溶液,分别于 0、2、4、6、8 h,按上述色谱条件,分别进样 10 μL,测定藁本内酯峰面积,其RSD为0.93%,表明样品溶液在至少8 h内稳定。
2.2.7 重现性考察 分别称取2 g同一中成药粉末(11号补肾益脑丸)5份,按“2.2.2”项下样品溶液制备方法制备5份供试液,按上述色谱条件,分别各进样10 μL,测定藁本内酯峰面积,其RSD=0.95%,表明该分析方法的重现性良好。
2.2.8 回收率实验 分别称取1 g同一中成药粉末(11号补肾益脑丸)6份,分别精密加入106 μg/mL藁本内酯对照品溶液各 0.5、0.5、1.0、1.0、2.0、2.0 mL,按“2.2.2”项下样品溶液制备方法制备加样回收供试品溶液,并按“2.2.3”项下色谱条件进行测定,计算回收率,结果藁本内酯的平均回收率为99.20%,其RSD为0.53%,结果见表1。

表1 藁本内酯加样回收率结果(n=6)
2.2.9 样品测定 分别取“2.2.2”项下制备好的各样品溶液,按“2.2.3”项下色谱条件,进样 10 μL,测定,记录藁本内酯峰面积,用外标法计算其藁本内酯的含量,结果见表2。
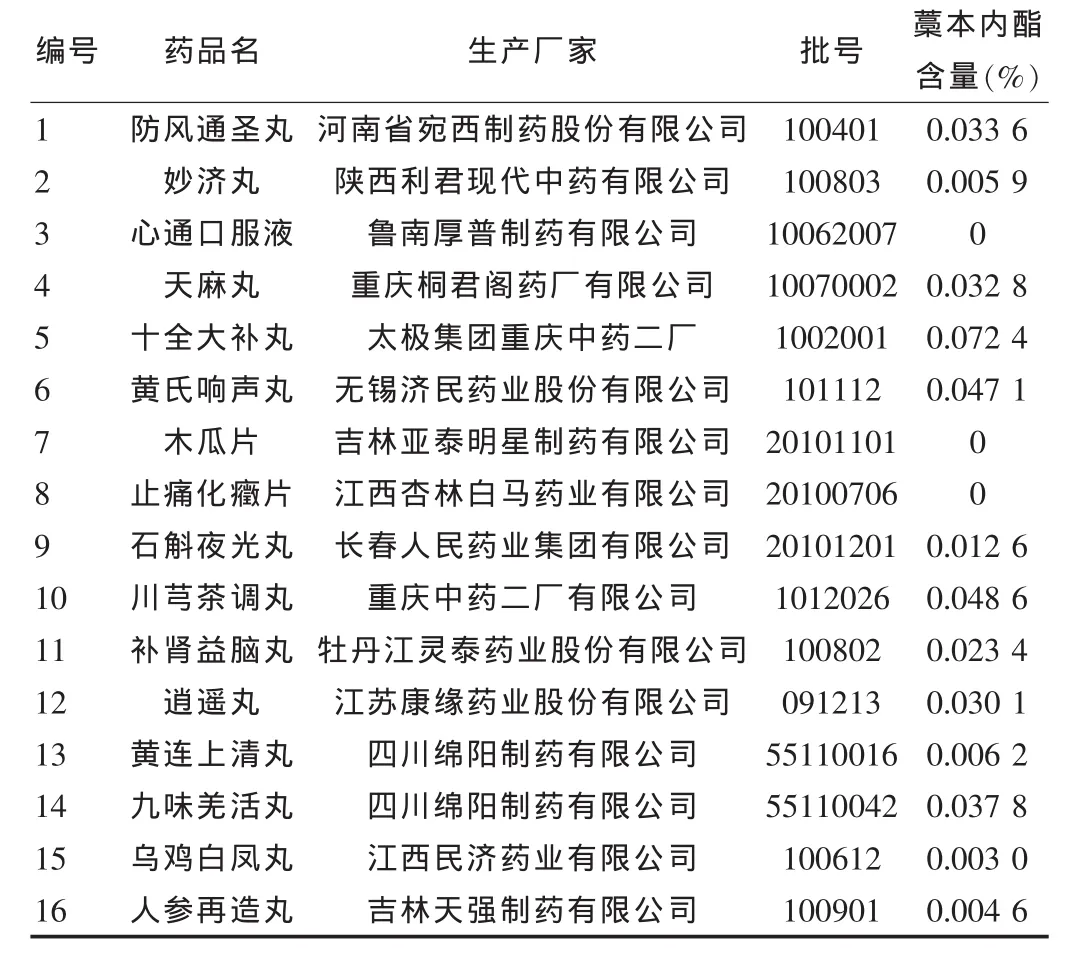
表2 各中成药中藁本内酯的含量测定结果(n=3)
从表2可以看出3、7、8号中成药中藁本内酯含量为0,此结果与薄层色谱中3、7、8没有检测到藁本内酯斑点相吻合;在2、13、15、16号样品中成药中检测到藁本内酯含量比起其他中成药要低约10倍,此与薄层色谱中2、13、15、16号样品几乎检测不到藁本内酯斑点的结果也相吻合;其他各中成药中藁本内酯的含量各有不同。
3 讨论
据文献研究报道[13]藁本内酯纯品的稳定性较差,特别是在室温下放置极易异构化。本实验参阅文献[8]并通过反复验证,发现藁本内酯在甲醇中稳定性良好,因而选用甲醇为各中成药的提取溶剂。本实验对藁本内酯薄层层析条件进行了系统的筛选,最终选用硅胶HF254板为吸附剂,以常用的紫外光灯为检测手段,以毒性很低、价格便宜的石油醚和乙酸乙酯系统为展开剂,该系统对藳本内酯有较好的展开分离。此方法简单方便,快捷低毒,十分适合于中成药中藁本内酯的快速定性检测。在建立HPLC方法时,笔者在参照前期建立HPLC测定川芎中藁本内酯研究的基础上[8],进一步对色谱条件及其方法学进行了系统考察研究,证实所选的色谱系统适用性好,结果可靠,其方法适用于成分复杂的中成药中藁本内酯的定量分析检测。
法定的当归、川芎药材检测指标成分是阿魏酸和川芎嗪,但在其药材中阿魏酸和川芎嗪的含量远低于藁本内酯,因此检测藁本内酯才能更加真实反应出中成药中当归、川芎的含量情况。本实验选用市面上含川芎、当归的常用中成药,对比薄层层析定性检测和高效液相定量检测结果,发现薄层层析没能检测出藁本内酯的中成药,在高效液相色谱法却能够检测到微量的藁本内酯,因此在此类药品鉴定中不仅要定性检测藁本内酯,也需要对其进行定量分析。本文最终建立了藁本内酯在中成药中的薄层色谱定性检测和高效液相色谱的定量分析方法,方法简便、准确、重现性好,适用于藁本内酯的检测分析,为含川芎、当归成分的中成药中藁本内酯的含量测定提供了参照,也为该类中成药质量控制提供了新的检测方法。
[1]国家药典委员会.中国药典[S].一部.北京:化学工业出版社,2005:28.
[2]孔亮,于志远,邹汉法,等.高效液相色谱与质谱联用分析测定川芎中有效成分阿魏酸与藁本内酯[J].分析化学,2004,32(11):1421-1424.
[3]Li SL,Chan SK,Lin G,et al.Simultaneous analysis of seventeen chemical ingredients of ligusticum chuanxiong by on-line high performance liquid chromatogramphy-diode array detector-mass spectrometry[J].Planta Med,2003,69:445-449.
[4]赵奎君,钟萌,谢俊大.不同产地当归中阿魏酸、藁本内酯及总多糖含量比较[J].中国中医药信息杂志,2007,12(14):37-39.
[5]Lu GH,Chan K, Chan CL.Quantification of ligustilides in the roots of Angelica inensis and related umbelliferous medicinal plants by highperformance liquid chromatography and liquid chromatography-mass spectrometry[J].Journal of Chromatography A,2004,1046:101-107.
[6]谢京晶,于珥,王一涛,等.HPLC法同时测定当归药材中6种成分的含量[J].药物分析杂志,2007,27(9):131-134.
[7]王婕,赵建邦,宋平顺.30批当归中阿魏酸、藁本内酯含量测定[J].中国实验方剂学杂志,2011,17(16):70-73.
[8]汪程远,张浩,钱忠明.HPLC测定不同川芎药材中藁本内酯[J].中草药,2006,37(3):447-449.
[9]石力夫,郑晓梅,秦溱,等.藁本内酯分解前后川芎挥发油对兔球结膜微循环影响的比较[J].中国药理学与毒理学杂志,1995,9(2):157-159.
[10]杨鹏远,张卫东,苏娟,等.藳本内酯用于防治动脉粥样硬化的用途:中国,CN 200310108859.6[P].2004.
[11]Zhao XX.Ligustilide extracted from Dang Gui composition for treatment and prevention of gynecological disease:US,US 2002-87073[P].2003.
[12]Cui F,Feng L,Hu J.Factors affecting stability of Z-Ligustilide in the volatile oil of radix angelicae sinensis and ligusticum Chuanxiong and its stability prediction[J].Drug Development and Industrial Pharmacy,2006,32:747-751.
[13]李桂生,马成俊.藁本内酯的稳定性研究及异构化产物的GC-MS分析[J].中草药,2000,31(6):405-409.
[14]汪程远,钱忠明,杜俊蓉.藁本内酯的研究进展[J].中国药学杂志,2006,4(12):889-891.
