阿奇霉素片在beagle犬体内的药代动力学研究
2009-04-26韩平
韩 平
【摘要】目的 研究阿奇霉素片在beagle犬体内的药代动力学。方法 10只beagle犬单次口服500mg/kg,服药后0~216 h间隔内定时采集血样,应用高效液相色谱-串联质谱仪联用测试样品浓度,梯形面积法计算药代动力学参数。结果 主要的药代动力学参数:Ke为(0.013±0.005)h-1,t1/2为(65.6+36.57) h, tmax为(3.80±4.80) h, Cmax为(455.2±222.8) ug·L-1,CL/F为(0.49±0.16 ) L·(h·kg)-1,AUC0-216和AUC– 分别为(9296.9±2285.9) mg·h·L-1和 (11242.5±3751.9) mg·h L-1。结论 该方法灵敏度高、快速、简便、无杂质干扰,适合于阿奇霉素浓度检测以及生物等效性研究。
【关键词】阿奇霉素片;高效液相色谱-串联质谱;药代动力学
Study on the Pharmacokinetics of AzithromycinTablet inBeagleDogs HAN Ping .(Department ofPharmacy ,Eerduosi Center Hospital, Eerduosi017000,China)
【Abstract】Objective To study the pharmacokinetics of azithromycin tablet in beagle dogs.Methods Ten beagle dogs were given a single oral dose of 500 mg/kg azithromycin tablet. The serum concentrations of azithromycin were determined by LC-MS/MS. The pharmacoki-netic parameters were calculated by DAS program.Results The main pharmacokinetic parameters of azithromycin for orally administered tablet were as follows: Ke is (0.013+0.005) -1 h,t1/2为is (65.6+36.57)h, tmax is (3.80+4.80) h, Cmaxis (455.2+222.8) ug·L-1, CL/F is (0.49+0.16 ) L·(h·kg) -1, AUC0-216and AUC– is(9296.9+2285.9) mg·h·L-1and (11242.5+3751.9) mg·h L-1.Conclusion This is a senstivquick methodthat fit to determine the serum concentrations of azithromycin.
【Key words】Azithromeycin tablet; LC-MS/MS; Pharmacokinetics
【中图分类号】R969.1
【文献标识码】A
【文章编号】1814-8824(2009)-03-0006-03
阿奇霉素(azithromycin )是新一代大环内酯类抗生素,特点是耐胃酸,口服吸收好,体液、组织分布广泛,半衰期长。临床广泛用于呼吸道、泌尿生殖系统及皮肤软组织感染的治疗,对革兰阴性菌、厌氧菌及细胞内病原体等抗菌活性优于红霉素和氟罗沙星。为此,本试验对其药代动力学进行研究,为临床用药提供参考。
1 药品、试剂与仪器
药品及试剂:阿奇霉素片,规格:每片250 mg,批号:030901,上海现代浦东药厂有限公司;阿奇霉素标准品(Azithromycin,纯度>99%,中国药品生物制品检定所提供,批号:200202-200702);甲醇及乙腈均为色谱纯;磷酸二氢钠、氯仿和正己烷均为分析纯。
仪器:API-3000型三重四极杆串联质谱仪,配有离子喷雾离子源以及Analyst 1.4.2数据处理系统,美国Applied Biosystem公司;Agilent 1200高效液相色谱输液泵,自动进样器,美国Agilent公司;色谱柱为Zorbax extend C18柱(2.1×150 mm I.D.,5μm粒径),美国Agilent公司
2 实验动物
Beagle犬,普通级,共25只,雌雄兼有,按体重随机分组,动物月龄:6~7个月,动物体重:8.5~10 kg,动物来源:军事医学科学院实验动物中心,实验动物合格证号:SCXK-(军)2002-001,动物房:实验动物使用许可证号,SYXK-(军)2002-001。
3 给药方法及血样采集
禁食12 h,口服给药,具体方法如下:给药日早晨空腹给药1次,用一小块馒头将胶囊包住,将犬嘴扳开,用手将包有胶囊的馒头送入犬后咽部,将犬嘴关闭,确认咽下后将嘴松开。服药后4h再进食。分别于服药前0及服药后0.5,1.0,2.0,3.0,4.0,6.0,8.0,12.0,24.0,48.0,96.0,144.0 h,采集前肢静脉血6 mL,置肝素抗凝管中;转速3 000 r·min-1离心10 min,分离出血清;置-20℃冰箱保存,待测。
3.1 色谱条件 色谱柱:Zorbax Extend-C18柱(2.1×150 mm,5μm);流动相:甲醇(0.4%甲酸):水(0.4%甲酸) = 9:1(v/v);流速:0.3 ml·min-1;柱温:40℃;进样量:20 μL。
3.2 质谱条件 离子源:离子喷雾离子化源;离子喷射电压:1800 V;温度:400℃;源内气体1(GS1,N2)压力:65 p.s.i;源内气体2(GS2,N2)压力:55 p.s.i;气帘气体(N2)压力:15 p.s.i;正离子方式检测;扫描方式:选择离子反应监测(MRM)方式;用于定量分析的离子对为m/z749.7→ m/z 591.6(阿奇霉素)和m/z 515.4→m/z 276.0(替米沙坦,内标)。
4 方法学考察
4.1 标准曲线的制备阿奇霉素:取Beagle犬空白血浆50 μL,依次加入阿奇霉素标准系列溶液50 μL , 配制成相当于血浆浓度为10,25,50,300,100,200,400和800 μg·L-1的血浆样品,每点为5样本,按“血浆样品的分析方法”项下操作,取20 μL进行LC/MS/MS分析,记录色谱图;以待测物浓度为横坐标,待测物与内标物的峰面积比值为纵坐标,用加权(W=1/χ2)最小二乘法进行回归运算,得阿奇霉素标准曲线。y = 0. 0042 x + 0. 0546,相关系数r = 0. 9993, 线性范围为3. 91 ~1 000 μg·L -1,最低定量限为3. 91μg·L-1。
4.2 专属性 在本色谱条件下测得色谱图
A 空白血浆色谱图
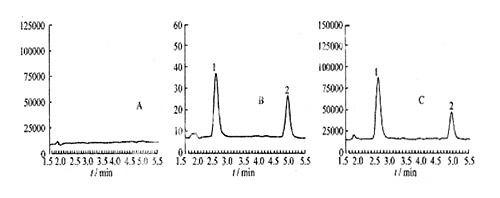
B 空白血浆中加入内标替米沙坦5ug·L-1、阿奇霉素50 ug·L-1的色谱图
C 4号受试犬服用阿奇霉素4 h后的血浆样品色谱图
(1代表阿奇霉素;2代表替米沙坦)
4.3 精密度 本法测定犬血浆中阿奇霉素血药浓度的日内、日间精密度均<10%,符合生物样品分析测定的要求 。阿奇霉素低25(μg·L-1)、中100(μg·L-1)、高400(μg·L-1)三个浓度的提取回收率(n=5)分别为98.48%、96.02 %和96.4 %。
4.4 药-时曲线图

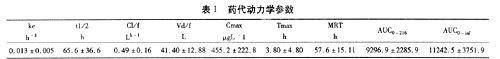
4.5 药代动力学参数 见表1。
5 讨论
考虑阿奇霉素分子结构无强紫外吸收的基团和自身试验条件,本研究建立了LC-MS/MS法测定犬血浆中阿奇霉素的浓度。与国内外其他测定方法相比具有以下特点:①与国内普遍采用的微生物测定干扰少。②与HPLC2UV 测定法相比其定量下限低可达到3.91 μg·L-1,而HPLC2UV法[3]检测的定量下限只有50μg·L-1,无法满足人体药动学及生物等效性研究的要求。③与电化学检测法相比,质谱检测对试剂、试验周边环境的要求较低,电化学检测器过于灵敏易受多种外界因素干扰。
参考文献
1 Gandhlr, Kaul CL, Panchagnula R. Pharmacokinetic valuation of an azithromycin controlled release dosage form in healthy human volunteers: a single dose study[J]. Int J Pharm, 2004, 270(122) : 128.
2 Rodvold KA, Danzlger LH, Gotfr Ied MH. Steady state plasma and bronchopulmonary concentrations of intravenous levoflox acin and azithromycin in healthy adults[J]. Antimicrob Agents Chemi, 2003, 47 (8) :79-82.
3 Amsden GW, Gray CL. Serum andWBC pharmacokinetics of 1500 mg of azithromycin when given either as a single dose or over a 3 day period in healthy volunteers [J]. J Antimicrob Chemother,2001, 47 (1):66-68.
4 郑筱萸.化学药品和治疗用生物制品研究指导原则(试行)[M].中国医药科技出版社,2006:158-160.
5 曾经泽等.生物药物分析方法的质量控制[J].中国药学杂志,1995,30(11):692
6 钟大放. 以加权最小二乘法建立生物分析标准曲线的若干问题[J]. 药物分析杂志, 1996, 16(5):343-346.
7 李惠义,罗淑荣,周同惠.液相色谱-质谱联用技术及其在药物代谢研究中的应用[J].国外医学药学分册,1997,24:257-263.
8 Ermer J,VAgel M Application of hyphenated LC-MS techniquesin pharmaceutical analysis[J].Biomed Chromatogr,2000,12(4):38-40.
9 卫生部药典委员会. 中华人民共和国药典[M]. 二部. 2005年版. 北京:化学工业出版社, 2005,附录173.
