5-羟基奥美拉唑中间体的合成研究
2009-01-15李健陈礼勤陈昌云
李 健 陈礼勤 陈昌云
摘要 以化合物1(2,3-二甲基-5-氯甲基吡啶-N-氧化物)为原料,经化合物1与硝酸在90 ℃下经硝化得到化合物2,化合物2与无水乙酸钠在95 ℃下发生亲核取代反应得到化合物3,化合物3在75 ℃下发生水解同时与甲醇钠反应得到化合物5(2,3-二甲基-5-羟甲基-4-甲氧基吡啶)共4步反应,最终成功合成目标化合物并进行表征确认。
关键词 5-羟基奥美拉唑;2,3-二甲基-5-羟甲基-4-甲氧基吡啶;药物中间体;合成
中图分类号:R975+.6 文献标识码:B 文章编号:1671-489X(2009)33-0088-02
Synthesis of Intermedium of 5-Hydroxy Omeprazole//Li Jian, Chen Liqin, Chen Changyun
Abstract In this thesis, the total synthesis of 2,3-Dimethyl-5-hydroxymethyl-4-methoxy pyridine was investigated. It was synthesized in total four steps. Compound 1 was nitrated by HNO3 at 90 ℃ to give compound 2. Compound 2 was reacted with CH3COONa at 95 ℃ to give compound 3. Compound 3 was hydrolyzed and simultaneously reacted with CH3ONa at 75 ℃ to give compound 5 and it was characterized by NMR.
Key words 5-hydroxy omeprazole;2,3-Dimethyl-5-hydroxymethyl-4-methoxy pyridine;intermediate;synthesis
Authors address
1 College of Bio & Chemical and Environmental Engineering, Nanjing Xiaozhuang University, Nanjing,
211171, China
2 Dept. of Chemistry and Chemical Engineering, Nanjing University of Technology, Nanjing, 210009, China
奥美拉唑是瑞典阿斯利康(AstraZeneca)公司推出的治疗胃溃疡的特效药,是近年来研究的作用机制不同于H2受体拮抗作用的全新的抗消化性溃疡药。奥美拉唑在人体内的代谢主要通过P450同功酶中的CYP2C19和CYP3A4。前者使奥美拉唑代谢为5-羟基奥美拉唑(5-hydroxy omeprazole),而后者则代谢为奥美拉唑砜[1]。5-羟基奥美拉唑是奥美拉唑在人体内的一个重要代谢产物[2-4],有关它的合成尚无报道。
药物代谢产物和药设计与结构改造在国内日益引起人们的重视[5-7],药物代谢产物的成功合成将有可能获得一种更有效、更少副作用的药物分子,或者有重要意义的先导化合物,也为相关药物的临床研究和深入探讨该类化合物的构效关系,发掘其他创新候选药物化合物提供重要的依据。
作为奥美拉唑的重要代谢产物,5-羟基奥美拉唑的成功合成将具有十分重要的意义。该化合物的合成方法不但有其重要的科学价值,同时它的成功合成为研究与这些药物相关的生物利用度和生物等同性等提供了宝贵的参照标准品。
1 合成路线
化合物5(2,3-二甲基-5-羟甲基-4-甲氧基吡啶)是5-羟基奥美拉唑的重要中间体。本文以化合物1(2,3-二甲基-5-氯甲基吡啶-N-氧化物)为原料,经与硝酸在90 ℃下硝化得到化合物2;化合物2与无水乙酸钠在95 ℃下发生亲核取代反应得到化合物3;化合物3在75 ℃下发生水解同时与甲醇钠反应得到化合物5,共4步反应,最终成功合成目标化合物。合成路线如图1所示。
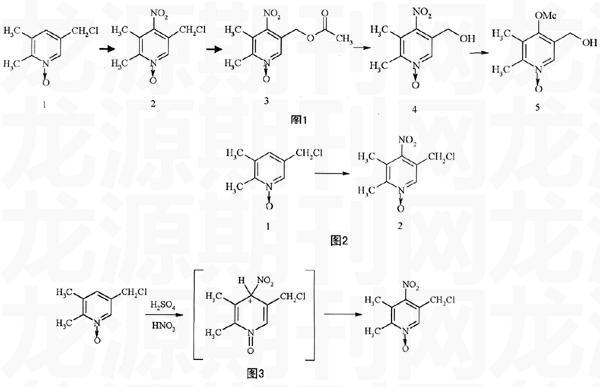
2 反应机理
2.1 由化合物1反应生成化合物2反应式如图2所示,反应机理如图3所示。
2.2 由化合物2反应生成化合物3反应式如图4所示,反应机理如图5所示。
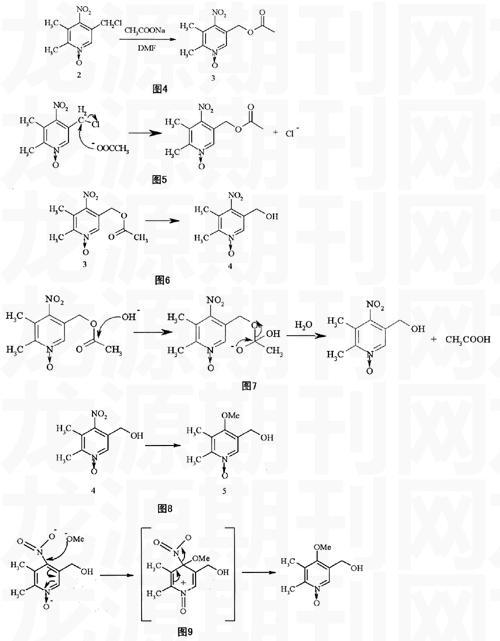
2.3 由化合物3反应生成化合物4反应式如图6所示,反应机理如图7所示。
2.4 由化合物4反应生成化合物5反应式如图8所示,反应机理如图9所示。
3 实验部分
3.1 化合物2(2,3-二甲基-5-氯甲基-4-硝基吡啶-N-氧化物)的合成(收率:77.2%)化合物1(18.0 g, 0.10 mol)冰浴中冷却,搅拌下滴加浓H2SO4(Ⅰ)(12.5 mL, 0.23 mol),缓慢升温至90 ℃。氮气保护下,400 rpm搅拌下,将上述混酸溶液缓慢滴加至反应中,滴加完毕后继续反应1小时。将反应在冰浴中冷却,搅拌下加入NaHCO3,中和至pH=8。所得黄色粘稠状固体用CH2Cl2(4×150 mL)萃取,有机相用无水Na2SO4干燥,经过滤、减压蒸干后得17.5 g橘黄色油状化合物2。
3.2 化合物3(2,3-二甲基-5-乙酸甲酯基-4-硝基吡啶-N-氧化物)的合成(收率:75.7%)化合物2(12.0 g,0.055 mol)溶于DMF(120 mL)得棕色溶液。加入无水CH3COONa固体(5.5 g,0.066 mol),氮气保护下,95 ℃搅拌30 min。将反应减压蒸干除去大部分DMF后,溶于去离子水(50 mL)中,用CH2Cl2(3×100 mL)萃取,所得有机相合并,经无水Na2SO4固体干燥,蒸干得10.6 g深棕色油状化合物3。
3.3 化合物5(2,3-二甲基-5-羟甲基-4-甲氧基吡啶-N-氧化物)的合成(收率:78.7%)化合物3(10.0 g,0.042 mol)溶于无水MeOH(Ⅰ)(100 mL)中,搅拌下加入NaOCH3的MeOH溶液,氮气保护下75 ℃油浴中加热回流1小时得深棕色化合物4溶液。反应置于冰浴中冷却,搅拌下用酸中和至pH=9,蒸干得25 g棕色泥状物。柱色谱分离得6.0 g晶体状化合物5。
化合物5 1HNMR(300 MHz, CDCl3):δ 2.23(s, 3 H),2.50(s, 3 H),3.80(s, 3 H),4.69(s, 2 H),8.23(s, 1 H)。
4 结论
经过4步反应并进行分离后,最终得到目标化合物5,并通过1HNMR表征确定所得产物即为目标化合物:2,3-二甲基-5-醇甲基-4-甲氧基吡啶-N-氧化物,总收率为46.0%。
参考文献
[1]赵焱.口服S-奥美拉唑胶囊药代动力学及奥美拉唑消旋体和代谢物的手性分离分析方法研究[D].成都:四川大学,2005
[2]Li J J,Johnson D S,Sliskovic D R,Roth B D.Contemporary drug synthesis[M].Wiley-interscience,2004
[3]Carr A A,Kinsolving C R.Olefinic 4-Substituted Piperidino Derivatives[P].US 387217,1975
[4]Baltes E,Lannoy J,Rodriguez L.2-(4-(Diphenylmethyl)-1-Piperazinyl)-Acetic Acids And Their Amides[P].US4525358,1985-06-25
[5]赵冬梅,李燕,卢业竑.药物代谢研究在新药开发中的作用[J].药学学报,2000,35(2):156-160
[6]阿基业,王广基.药物代谢研究与药物设计及结构修饰[J].药学进展,2002,26(2):80-86
[7]刘昌孝.代谢物组学在中药现代研究中的意义[J].天津药学,2005,17(2):1-6
